Пациенты после операции рака гортани

Уровень заболеваемости раком гортани в настоящее время составляет 4,6 на 100 000 населения. За последние 10 лет установлено снижение заболеваемости у мужчин на 2,8% и прирост заболеваемости на 18,2% у женщин [1, 2].
Несмотря на широкие возможности современной диагностики, большинство (60-70%) больных раком поступают на лечение в III и IV стадиях заболевания, и только 30-40% – в I и II стадиях [1-3].
При T1 и T2 стадиях заболевания, а у ряда больных – и при T3 возможно выполнение функционально-сохраняющих операций [4-20].
Основным видом лечения распространенных опухолей гортани является ларингэктомия, которая приводит к потере голоса [2, 3, 12, 20-41].
Проблема диагностики, лечения и реабилитации больных раком гортани диктует необходимость междисциплинарного подхода и взаимодействию врачей разных специальностей [2, 3].
При выборе метода лечения, объема хирургического вмешательства важнейшим аспектом является точная диагностика опухоли, ее распространенность, особенно при выполнении резекций гортани [2-5, 8]. Поэтому этой категории больных, кроме общеклинических исследований, осмотра, пальпации, проводятся инструментальные исследования: непрямая ларингоскопия, фиброларингоскопия, боковая рентгенограмма и томограммы, МСКТ, УЗИ гортани и лимфатических узлов [42], цитологическое и гистологическое исследования. УЗИ гортани, кроме эндоларингеального распространения, позволяет выявить распространение опухоли на щитовидный и перстневидный хрящи, щитовидную железу, мягкие ткани шеи и подтвердить злокачественное образование путем пункции под контролем монитора и цитологическим исследованием полученного материала.
При планировании объема операции необходимо предусмотреть онкологическую адекватность хирургического вмешательства, восстановление функций гортани после различных видов резекций органа, а при выполнении ларингэктомии – реабилитацию голосовой функции с применением отечественных голосовых протезов (патент № 2446774) [43].
За последнее время разработаны различные варианты функционально-сохраняющих операций при раке гортани [4-11, 13-20]. Эти операции показаны, в частности, при распространении опухоли на переднюю комиссуру, гортанные желудочки, подскладковый отдел, эндофитных формах роста опухоли [4, 13, 14].
Как известно, вид резекции зависит от локализации опухоли. В зависимости от плоскости выполнения операции выделяют вертикальную и горизонтальную резекцию гортани.
При выполнении различных вариантов горизонтальной резекции в комбинации с резекцией валекул и корня языка в большей степени страдает защитная функция органа. При данном виде вмешательства не происходит изменения переднезадних размеров органа и сохраняется его хрящевой каркас [4, 8, 13, 14, 18]. У этой категории больных наряду с восстановлением дыхательной, голосовой функций важнейшим аспектом является восстановление защитной функции при отсутствии надгортанника. Декануляция больного возможна при восстановлении всех функций органа.
Вертикальную резекцию выполняют во фронтолатеральной плоскости с резекцией у ряда больных перстневидного, черпаловидного хрящей, первого и второго колец трахеи. При выполнении этой операции удаляют большие фрагменты щитовидного хряща во фронтолатеральной плоскости, что приводит к уменьшению передне-заднего размера гортани и сужению просвета органа. Это диктует необходимость сложной одномоментной реконструкции с формированием просвета органа на силиконовом эндопротезе [4-6, 8, 9, 13-15, 17, 18].
Ларингэктомия позволяет радикально удалить опухоль, однако приводит к инвалидизации пациента. При этом дыхание осуществляется через концевую трахеостому. После такой операции важное значение приобретает реабилитация голосовой функции с помощью логопедических методик, голосообразующих аппаратов и реконструктивно-пластических операций [2, 3, 12, 20-23].
Основным принципом восстановления голоса после ларингэктомии является индивидуальный подход и выбор пациентом метода реабилитации. Наиболее предпочтительным вариантом является овладение больным всеми тремя методиками восстановления голоса и их использование в зависимости от обстоятельств.
В настоящее время разработаны хирургические методы восстановления голоса после полного удаления гортани, основанные на принципе шунтирования, т. е. создания соустья между глоткой и трахеей, пищеводом и трахеей [14, 20-31, 33, 36-39].
Трахеопищеводное шунтирование получило развитие в 2 направлениях: формирование шунта за счет аутотканей и протезирование трахеопищеводного шунта. Трахеопищеводное шунтирование за счет аутотканей направлено на формирование защитного клапанного механизма. Эта операция позволяла восстановить голосовую функцию после ларингэктомии у 86,2% больных, а защитную – у 71,7%. Нарушения функции защиты трахеопищеводного шунта почти у 30% больных указывали на необходимость создания шунта и клапана со стабильными размерами, т. е. голосового протеза [14]. За последние 25 лет в нашей стране применяются различные протезы для восстановления голосовой функции после полного удаления гортани (Singer-Bloom, Provox и т. д.)
В настоящее время созданы новые виды отечественных голосовых протезов разных размеров и оригинальной конструкции с более надежной фиксацией в трахеопищеводном шунте [43].
Цель работы – повышение эффективности реабилитации больных раком гортани после резекций органа и ларингэктомии.
Наш опыт основан на лечении 102 больных. Средний возраст составил 59,2±9,6 года. Мужчин было 94 (92,2%), женщин – 8 (7,8%). По нозологическим формам больные распределялись следующим образом: первичный рак гортани выявлен у 97: Т1N0M0 – у 8 (8,2%), Т2N0M0 – у 63 (65%), Т3N0M0 – у 18 (17,6%), T3N1M0 -у1 (0,9%), Т4N0M0 – у 3 (2,9%), Т4N1M0 – у 4 (3,9%), рак корня языка с распространением на вестибулярный отдел гортани – у 1, саркома гортани – у 1, рецидив рака после полной дозы лучевой терапии и органосохранных операций – у 3.
Резекция гортани выполнена у 83 человек, из них при первичном раке гортани – у 81 больного (T2N0M0 – у 64, T3N0M0 – у 10, T1N0M0 – у 8), раке корня языка с распространением на надскладочный отдел гортани – у 1, рецидиве рака после полной дозы лучевой терапии – у 1. Резекция гортани в вертикальной плоскости выполнена у 71 человека (фронтолатеральная резекция гортани – у 59 человек, расширенная фронтолатеральная – у 11, комбинированная – у 1). У 12 больных была выполнена горизонтальная резекция гортани.
Ларингэктомия с трахеопищеводным шунтированием и установкой отечественного голосового протеза проведена у 19 человек.
Большинство больных поступали на лечение в Т3N0-1M0 (10) и Т4N0-1M0 (6) стадиях заболевания. Кроме того, у 2 человек эти операции выполнены по поводу рецидива заболевания после функционально-сохраняющих вмешательств, и саркомы гортани – у 1 пациента. Одномоментное трахеопищеводное шунтирование с эндопротезированием выполнено у 17 больных, отсроченное – у 2.
Нами разработан алгоритм реабилитации больных раком этой локализации, который состоит из нескольких этапов.
На предоперационном этапе проводилась психологическая подготовка больного к лечению, коррекция сопутствующих заболеваний. Также важным аспектом является санация полости рта, обработка антисептическими растворами.
На интраоперационном этапе при выполнении органосохраняющих операций проводилась реконструкция оставшихся элементов органа, создание адекватного просвета гортани. С этой целью в просвет органа устанавливали эндопротез оригинальной конструкции. Протез представляет собой трубку, верхний конец которой имеет вид шатра с двумя боковыми отверстиями для дыхания. Крыша расположена так, что полностью перекрывает просвет трубки. Переднебоковая стенка гортани формируется над протезом с использованием передних мышц шеи или лоскута из корня языка.
При выполнении ларингэктомии с трахеопищеводным шунтированием и эндопротезированием на интраоперационном этапе важным аспектом является создание шунта таких размеров, чтобы голосовой протез плотно фиксировался в нем. При одномоментном протезировании после удаления гортани формировали концевую трахеостому, при которой моделировали языкообразный лоскут из задней стенки трахеи. После ларингэктомии глотку ушивали частично. Формировали нижние и боковые края трахеостомы, на заднюю стенку накладывали лигатуры. В нижние отделы глотки и пищевода вводилась защитная пластинка для предупреждения травмы задней стенки пищевода (рис. 1). С помощью троакара, отступя 7-8 мм от верхнего края задней стенки, производилась пункция трахеи и передней стенки пищевода (рис. 2). Через сформированный шунт проводили пластиковый катетер, на который надевали протез. Катетер прошивали иглой с помощью нити (лавсан № 5), при этом фиксировался сам катетер и голосовой протез (рис. 3). С помощью катетера протез устанавливали в трахеопищеводном шунте (рис. 4). Рану глотки и пищевода ушивали послойно, с введением назогастрального зонда.
 Рис. 1. Установка защитной пластины (описание в тексте).
Рис. 1. Установка защитной пластины (описание в тексте).
 Рис. 2. Пункция задней стенки трахеи и передней стенки пищевода.
Рис. 2. Пункция задней стенки трахеи и передней стенки пищевода.
 Рис. 3. Установка протеза в трахеопищеводный шунт с помощью проводника (описание в тексте).
Рис. 3. Установка протеза в трахеопищеводный шунт с помощью проводника (описание в тексте).
 Рис. 4. Голосовой протез установлен в трахеопищеводном шунте.
Рис. 4. Голосовой протез установлен в трахеопищеводном шунте.
Отсроченное трахеопищеводное шунтирование с эндопротезированием выполняли у больных, которые не смогли овладеть пищеводной речью и не имели противопоказаний.
Следующий этап реабилитации – послеоперационный. Его можно разделить на ранний (стационарный) и поздний (амбулаторный). На стационарном этапе проводилась консервативная терапия: антибактериальная, антигистаминные, нестероидные противовоспалительные препараты, ингаляционная терапия. Длительность стационарного этапа составляет 7-14 дней. Силиконовый эндопротез после резекций гортани удалялся на 14-21-е сутки.
Важнейшими аспектами в реабилитации больных после функционально-сохраняющих операций является не только восстановление функционального резерва гортани, но и предупреждение развития осложнений со стороны трахеи: грануляций, стеноза, трахеомаляции. С целью предупреждения осложнений со стороны трахеи мы используем атравматические варианты формирования трахеостомы между кольцами, подбор трахеостомических трубок адекватных размеров, санацию трахеи с применением ферментов, антисептиков и противовоспалительных препаратов. Кроме того, мы рекомендуем дышать через естественные пути методом временного или постоянного закрытия трахеостомической трубки обтуратором, проводить речевые тренировки. После восстановления дыхательной и защитной функций выполняется декануляция.
После выполнения горизонтальных резекций гортани одной из важнейших задач являлось восстановление защитной функции. В раннем послеоперационном периоде питание осуществляли через носопищеводный зонд с постепенными тренировками естественного акта глотания. Далее, при восстановлении функции глотания через естественные пути назогастральный зонд удаляли. В дальнейшем в трахею устанавливалась трубка типа Portex, и только на период приема пищи больному рекомендовано раздувать манжету. После восстановления функции защиты и при достаточном просвете органа выполняли декануляцию.
Большинству больных раком гортани в послеоперационном периоде проводили дистанционную гамма-терапию. В этот период для предупреждения лучевого эпителиита проводилась ингаляционная, десенсибилизирующая терапия и терапевтический лазер на область оперативного вмешательства.
Кроме того, в послеоперационном периоде мы применяли эндоларингеальную коррекцию просвета гортани с использованием эндоскопической техники и лазера. Этим больным проводилось поэтапное удаление лигатур, лазерная абляция грануляций и рубцовых тканей.
При планировании деканюляции просвет оперированной гортани оценивали с помощью фиброларингоскопии и УЗИ органа [60]. При отсутствии противопоказаний производилось ушивание трахеостомического отверстия. После деканюлации больные направлялись к логопеду для обучения звучной речи. Кроме того, после проведенного лечения нами выполнялся акустический анализ голоса. Запись речи проводили в тихом помещении, с использованием настольного микрофона Logitech, расположенного в 15-20 см от сидящего за столом диктора. Обработка звукового сигнала осуществлялась с помощью программы Praat. Анализ полученных данных показал, что у больных мужского пола, перенесших ларингэктомию с трахеопищеводным шунтированием и эндопротезированием, частота основного тона составила 90-250 Гц, интенсивность 49-62 дБ, время фонации 14-16 с. У больных, перенесших резекции гортани, частота основного тона составила 80-187 Гц, интенсивность 44-59 дБ, время фонации 18-20 с.
В послеоперационном периоде после ларингэктомии с трахеопищеводным шунтированием и эндопротезированием ежедневно проводилась санация ротовой полости антисептическими растворами, пациентам запрещалось проглатывать слюну. С целью укрепления кольца трахеопищеводного шунта выполнялась его обработка 5% раствором йода, ультразвуковая ингаляционная с антигистаминными препаратами на щелочной воде.
После заживления раны и удаления носопищеводного зонда больного обучали произносить звуки, делая глубокий вдох, и на выдохе, закрывая трахеостому. При этом поток воздуха направлялся в протез и пищевод. Больной мог произносить звуки, применяя перфорированную трахеостомическую трубку.
Для беглого произношения слов и уменьшения шумового компонента проводилась дыхательная гимнастика, при которой соотношение вдох/выдох должно соответствовать 1:3. При этом необходимо расслабление нижней челюсти, выбор позиции головы и выполнение артикуляционных упражнений.
Так как голосовой протез устанавливали в шунте между трахеей и пищеводом, он подвергался воздействию мокроты, пищи, слюны, пыли и т. д., что приводило к нарушению функции защитного клапана. Это требовало ежедневного ухода за ним. Для этого необходимо удалять со стенок протеза и с защитного клапана остатки пищи после каждого приема, корки с помощью специальной щетки, промывать антисептическими растворами (хлоргексидин, мирамистин, 3% перекись водорода и т. д.) и обрабатывать противогрибковыми препаратами [59]. Тщательная гигиена трахеопищеводного шунта и силиконового эндопротеза позволяла увеличить срок его эксплуатации. Средний срок службы отечественных голосовых протезов составил 18-20 мес, однако нами зафиксированы наблюдения четырех- и одиннадцатилетней его эксплуатации.
После проведенного лечения больные находятся на диспансерном наблюдении. В первый год после выполнения операций с целью выявления раннего рецидива рака гортани и метастазов необходимо каждые 1,5-2 мес выполнять пальпацию шеи, УЗИ, непрямую ларингоскопию, фиброларингоскопию (см. рис. 5 и 6) и трахеоскопию, общеклиническое обследование, рентгенографию легких 2 раза в год. В дальнейшем эти исследования проводятся через 3-6 мес.
 Рис. 5. Просвет гортани после горизонтальной резекции через 12 мес.
Рис. 5. Просвет гортани после горизонтальной резекции через 12 мес.
 Рис. 6. Просвет гортани после фронтолатеральной резекции гортани через 12 мес.
Рис. 6. Просвет гортани после фронтолатеральной резекции гортани через 12 мес.
Системный подход к реабилитации этой категории больных и разработанный нами алгоритм позволили восстановить функции гортани после органосохраняющих операций у 79 (95,2%) из 83 больных. Рубцовый стеноз органа имел место у 3 больных, трахеомаляция – у 1 человека, что потребовало формирования ларингостомы с установкой Т-образной трубки.
Голосовая функция у больных после ларингэктомии с трахеопищеводным шунтированием и эндопротезированием была восстановлена у 18 (94,7%) из 19 человек. Отсутствие голоса после операции наблюдалось у 1 больного вследствие спазма констрикторов глотки.
При диспансерном наблюдении в первый год после операции были выявлены односторонние регионарные метастазы у 5 больных с T3 и Т4 стадиями заболевания после комбинированного лечения. Им было выполнено футлярно-фасциальное иссечение лимфатических узлов и клетчатки шеи на стороне поражения. Кроме того, у 4 больных выявлен рецидив заболевания после комбинированного лечения рака гортани с выполнением функционально-щадящих операций, и у одного больного – рецидив заболевания после комбинированного лечения рака корня языка с распространением опухоли на вестибулярный отдел гортани после комбинированной горизонтальной резекции. Продолженный рост опухоли и рецидив заболевания выявлен в сроки от 6 мес до 5 лет. Ларингэктомия выполнена у 2 больных, химиотерапевтическое и симптоматическое лечение проведено у 3 человек.
Таким образом, системный подход к реабилитации больных раком гортани позволяет восстановить функции органа после функционально-сохраняющих операций у 95,2% больных; после полного удаления гортани с трахеопищеводным шунтированием и эндопротезированием с применением отечественных голосовых протезов – у 94,7% больных.
Конфликт интересов отсутствует.
Источник
Рак гортани ежегодно диагностируют у 7 тысяч россиян. Из-за малой осведомленности пациентов и врачей чаще всего заболевание выявляют уже на последних стадиях — в этом случае человеку грозит операция по удалению гортани и потеря голоса.
«Пространство равных возможностей» и социально-предпринимательский проект Everland запустили большой проект о раке гортани, чтобы поделиться опытом людей, которые уже пережили операцию. «Такие дела» поговорили с врачами и пациентами о том, как жить после потери голоса и какие есть пути его возвращения.
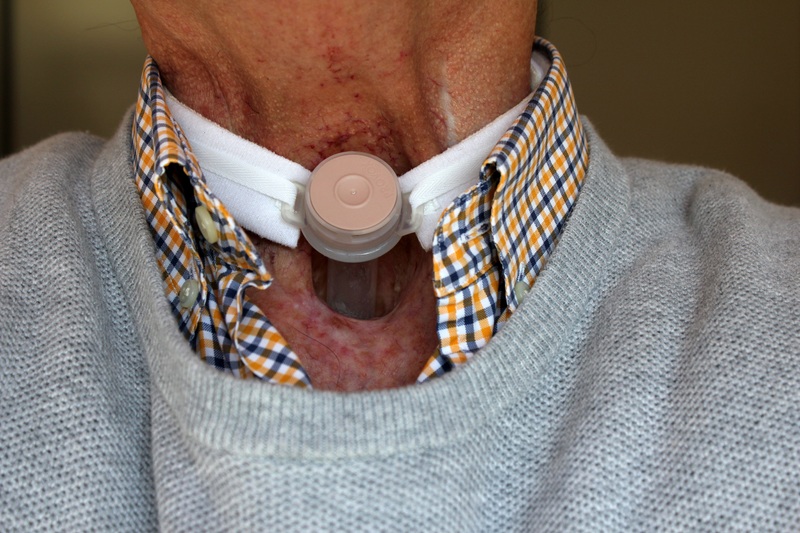 Фото: pxhere.com
Фото: pxhere.com
Человек теряет голос
В России рак гортани занимает 11-е место по распространенности среди других видов рака, ежегодно он диагностируется у 6,5–7 тысяч пациентов. Большинство людей с раком гортани — это мужчины 45–59 лет. Наиболее частые причины появления заболевания — курение и алкоголь.
Онколог, заведующий отделением опухолей головы и шеи Челябинского областного центра онкологии и ядерной медицины Александр Гузь говорит, что более чем в половине случаев рак гортани выявляется на III и IV стадиях, но в последнее время эта тенденция меняется в лучшую сторону.
Врач объясняет: пациенты долгое время не обращают внимания на свое состояние и не идут в поликлинику, потому что не знают симптомов рака гортани. «Достаточно долго пациенты имеют один-единственный симптом — осиплость голоса. Они не знают, что это может быть причиной злокачественного образования гортани. Простыл, заболел, съел мороженое, вирус перенес на ногах — люди находят, чем объяснить свои первые симптомы», — говорит онколог.
Александр Гузь указывает на низкую осведомленность врачей, в частности терапевтов, о заболевании. По словам эксперта, в своей обычной практике терапевты встречаются с раком гортани максимум раз в год и, поскольку это не самое распространенное заболевание, правильно интерпретировать симптомы не могут.
На III и IV стадиях заболевания одни из возможных вариантов лечения — это операция по удалению гортани или проведение химиолучевой терапии. В 2018 году российские врачи впервые смогли восстановить пациенту удаленную гортань с помощью фрагментов кишечника. В будущем такие операции позволят людям нормально есть и разговаривать. Сейчас же, когда пациенту удаляют гортань, он лишается возможности говорить звучным голосом.
Восстановление голоса
После удаления гортани у человека есть несколько вариантов начать говорить: развитие пищеводного голоса, установка голосового протеза или электронной гортани. Реабилитационные мероприятия по восстановлению голоса можно проводить не раньше 14 суток после операции и только после разрешения лечащего хирурга.
По словам логопеда Татьяны Петровой, некоторые люди вообще не хотят общаться после операции. «Человек теряет голос и вообще возможность произносить какие-либо звуки, соответственно, становится психологически подавленным. Некоторые становятся агрессивными, уходят в себя», — отмечает Петрова.
Логопед вспомнила историю своей пациентки, которая до операции была педагогом начальных классов, а после решила уехать из города в деревню и не восстанавливать свой голос. Через год позвонила дочь пациентки и сказала, что ее матери удалось произнести какие-то слова. Семья поверила, что вернуть голос возможно, и начала заниматься реабилитацией. «Я только показала ей технику пищеводного голоса, и она у меня зазвучала практически с первых занятий», — вспоминает Петрова.
По ее словам, самую главную роль в восстановлении голоса играет желание. «Если нет желания, никакой родственник не сможет помочь пациенту, кроме него самого. Если человек сам хочет, это в 99% случаев означает успех», — считает логопед.
Александр Гузь тоже говорит, что не все пациенты решают заниматься возвращением голоса после операции по удалению гортани. «У некоторых людей нет такой глобальной потребности разговаривать. Такие пациенты у нас есть, которые молчат себе и молчат. Они учатся что-то шептать, окружающие их понимают, а большего им и не надо», — отмечает онколог.
Пищеводный голос
Методика восстановления голоса подбирается индивидуально. «Кому-то подойдет только электрогортань, потому что бывают разные объемы операции и вызвать пищеводный голос может быть невозможно. Для тех пациентов, которые довольно активны и которым нужно быстро общаться, подойдет голосовое протезирование. Если пациенты терпеливые, то их можно обучить пищеводному голосу, потому что это работа не одного дня», — объясняет логопед Петрова.
По словам Александра Гузя, пищеводный голос считается самым простым для пациентов способом. В отличие от протеза и электронной гортани он не требует дополнительных приспособлений и проведения операции, а при разговоре не задействуются руки. Звук образуется в результате выхода накопленного в желудке воздуха через часть пищевода.
Развитие пищеводного голоса зависит от воли пациента: ему предстоит длительное (до шести месяцев) обучение с фониатром или логопедом, а также самостоятельные занятия. Среди минусов пищеводного голоса Гузь называет сложность освоения. Кроме того, произносить длинные предложения таким способом не получается, потому что не хватает воздуха.
Эвелине Роговой провели операцию в 2015 году, и врачи сразу посоветовали ей развивать пищеводный голос. «Когда мне сделали операцию, профессор буквально сразу сказал: начинай читать. Я сначала вылупила глаза, а потом поставила себе цель, что я не буду молчать. И я начала потихоньку говорить какие-то обычные слова», — вспоминает Рогова.
Она научилась разговаривать пищеводным голосом через несколько недель тренировок. Так она общалась на протяжении двух лет, знакомые хорошо ее понимали, трудности возникали лишь при общении по телефону — пищеводный голос тише обычного. Однако из-за бронхиальной астмы Рогова начала задыхаться и ей стало тяжело говорить, в итоге женщина решилась на установку голосового протеза. «У меня выбора не было — либо молчать, либо мучиться, поэтому пришлось поставить протез», — говорит Рогова.
Голосовой протез
У голосового протеза есть свои особенности: при разговоре человеку необходимо задействовать руки, чтобы закрывать выход воздуха из трахеостомы. Каждые несколько месяцев протез нужно менять, за ним нужно ухаживать и ежедневно чистить его. Онколог Гузь указывает, что поэтому протез не подойдет людям, которые имеют проблемы со зрением и с координацией движений.
Некоторым пациентам после установки голосового протеза требуется помощь в «разработке» и освоении нового голоса, они нуждаются в непродолжительных занятиях с логопедом или фониатром. Стоимость протеза составляет около 30 тысяч, пациенты могут добиться возмещения покупки от государства, но лишь постфактум.
Ирина Аралова рассказывает, что главная проблема в голосовом протезе, с которым она ходит уже 13 лет, — это то, что его приходится часто менять, при этом государство в этом ей почти не помогает. Ирина говорит, что первый протез прослужил ей два года, а сейчас приходится менять его каждые 3–6 месяцев. «Сколько прослужит голосовой протез, точно сказать нельзя, — отмечает Аралова. — Протез разрушают грибки, которые со временем на нем селятся. Как быстро это произойдет, зависит от многих причин: иммунитета, питания, ухода за протезом».
Женщина установила протез лишь спустя два года после операции, поскольку изначально ей никто не сказал, что они вообще существуют. Аралова обратилась в Московскую онкологическую больницу № 62 к доктору медицинских наук Елене Новожиловой, которая была в числе первых хирургов-онкологов в России, устанавливающих голосовые протезы. Новожилова не только проводит операции, но и помогает пациентам в реабилитации, в том числе организовала хор пациентов с протезами.
По словам Араловой, после установки протеза ее голос почти не изменился, а говорить она начала сразу. Женщина рассказала, что она вместе с другими пациентами создала специальную группу в WhatsApp, чтобы поддерживать людей, которым только предстоит операция. «Некоторые люди боятся оставаться без голоса и делать операцию. Мы говорим, что жизнь на этом не заканчивается», — объясняет Аралова.
Электронная гортань
Голосообразующий аппарат — электронную гортань — можно установить без операции. Он представляет собой небольшой прибор, похожий на микрофон, который прикладывается к шее и вместо гортани создает вибрацию. Денис Смоляков, который пользуется голосообразующим аппаратом, называет еще один его минус: прибор нуждается в зарядке каждые 1–2 недели. Если электронная гортань внезапно разрядилась, нужно искать батарейку.
Некоторые пациенты отказываются от электронной гортани, так как речь с этим прибором получается монотонной и роботизированной. Жена Дениса, Юлия Филиппова, говорит, что сама она уже не замечает, что ее муж говорит «как-то иначе». «Бывает, что люди на улице обращают на Дениса внимание. Ну оглянется, удивится и отвернется, поняв, что сзади него находится не робот, и дальше пойдет», — говорит Филиппова.
Денис сказал первое слово сразу в магазине, во время покупки аппарата. Через неделю он начал медленно соединять слова в предложения, а уже через два месяца в совершенстве освоил аппарат и разговаривал по телефону. Через некоторое время Смоляков выступал с трибуны, рассказывая свою пациентскую историю на конгрессе онкологических пациентов. «У нас дети, внуки, мама, сестра, племянницы — хочешь не хочешь, но ты заговоришь. Все спрашивали его совета и хотели поговорить с ним. Одиноким сложнее, человек говорит, когда есть кому его слушать», — рассказывает Филиппова.
Женщина считает электронную гортань оптимальным методом восстановления голоса: для нее нет противопоказаний и она не грозит осложнениями. Государство компенсирует покупку голосообразующего аппарата раз в пять лет. Сумма, которую оно выделяет, фиксированная — около 17 тысяч рублей. Это средняя стоимость российского аппарата, поэтому, если пациенты покупают зарубежный прибор, который на порядок дороже, разницу приходится доплачивать самим.
Филиппова считает, что при выборе методики восстановления голоса нужно ориентироваться на советы врача, финансовые возможности и образ жизни. «Например, если человек работает в компании и требуется постоянное общение с большим количеством людей, то ему будет легче пользоваться протезом, так как голос максимально приближен к естественному. Но если он живет в деревне, вдали от врачей, то установка протеза будет затруднена», — говорит женщина.
Источник