Литература по стенозу гортани
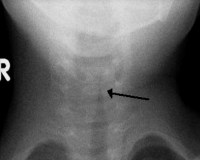
Стеноз гортани у детей — это сужение просвета органа вплоть до полной его закупорки, что сопровождается нарушением внешнего дыхания. Состояние развивается при ложном крупе, травматических и аллергических поражениях гортани, как следствие длительного периода интубации. Симптомы стеноза включают одышку, бледность и синюшность кожных покровов, повышенную потливость. На стадии декомпенсации возникают судороги, потеря сознания, остановка дыхания. С диагностической целью проводят ларингоскопию, МРТ и КТ гортани, эндоскопическое обследование. Лечение в основном хирургическое: коникотомия или плановые коррекции рубцовых изменений.
Общие сведения
Стеноз является осложнением болезней дыхательной системы или других органов, он не возникает изолированно на фоне полного здоровья (за исключением травм и аспирации инородных тел). Симптомы чаще наблюдаются у грудничков и детей раннего возраста, что обусловлено анатомо-функциональными особенностями верхних дыхательных путей. Заболевание является серьезной проблемой в современной отоларингологии, поскольку при тяжелых формах сужения и отсутствии неотложной медицинской помощи смертность достигает 90-100%.

Стеноз гортани у детей
Причины
Зачастую стеноз гортани у детей осложняет течение острого ларингита, вызванного вирусом парагриппа. При этом формируется ложный круп, при осложненном течении которого сужаются воздухоносные пути. Патология характерна для пациентов до 5-6 лет. Симптомы стеноза могут развиваться при других воспалениях (эпиглоттит, дифтерия). Невоспалительными причинами перекрытия гортани служат:
- Инородные тела. В раннем возрасте дети могут проглатывать бусины, пуговицы и другие мелкие предметы. Ввиду узости гортани посторонние тела застревают в области голосового аппарата, перекрывая доступ воздуха и вызывая симптомы удушья.
- Травма. Механическое воздействие на шею при падении, ударе, удушении сопровождается повреждением гортанных хрящей, тяжелыми нарушениями вентиляционной функции. Подобные травмы представляют угрозу для жизни детей, особенно при их сочетанном характере.
- Аллергия. В детском возрасте стенки гортани очень рыхлые, поэтому при иммунном воспалении они реагируют массивный отеком. При аллергической реакции немедленного типа симптомы полного перекрытия просвета у детей наступают за несколько минут.
- Длительная ИВЛ. Проблемой детской отоларингологии остаются рубцовые постинтубационные стенозы которые при отсутствии адекватного и комплексного лечения приводят к инвалидизации и социальной дезадаптации детей. Сужение становится осложнением «гортанного пролежня».
Частому развитию стеноза способствуют анатомо-физиологические особенности детской гортани. Она имеет короткое преддверие, малый диаметр и податливый хрящевой скелет, что создает благоприятные условия для сужения просвета и даже его полного перекрытия. У детей отмечаются симптомы гипервозбудимости рефлексогенных зон и повышенный тонус парасимпатической системы, с чем связана быстрая реакция мышц, замыкающих голосовую щель в ответ на раздражение.
Патогенез
Формирование стеноза у детей обусловлено тремя компонентами: отеком гортанной слизистой, спазмом мускулатуры и закупоркой просвета густыми слизистыми выделениями. Затруднение прохождения воздуха создает нарушения аэродинамики и увеличивает сопротивление воздушному потоку, провоцирует типичные симптомы (одышку, чувство нехватки воздуха). Недостаточное поступление кислорода сопровождается гипоксией и гипоксемией, кардиоваскулярными и мозговыми нарушениями.
Классификация
С учетом времени появления стенозы подразделяются на врожденные и приобретенные. По локализации бывают синехии заднего или переднего отдела, кольцевидные рубцовые изменения, тотальное заращение просвета. По размеру поражения выделяют ограниченный рубцовый стеноз (до 10 мм) и распространенную форму. В клинической практике наиболее важна классификация по тяжести течения, согласно которой выделяют 4 стадии:
- I (компенсация). Чтобы обеспечить адекватное дыхание, в процесс вовлекается вспомогательная мускулатура, но ЧДД в норме и состояние ребенка удовлетворительное.
- II (субкомпенсация). Происходит чрезмерное напряжение компенсаторных механизмов, в результате чего функция внешнего дыхания нарушается, возникает легкая степень гипоксии.
- III (декомпенсация). Характеризуется полным срывом адаптационных механизмов, тяжелыми расстройствами дыхательной функции и патологическими изменениями гомеостаза.
- IV (асфиксия). Жизнеугрожающее состояние, проявляющееся остановкой дыхания с соответствующими расстройствами кардиоваскулярной системы.
Симптомы
Основной признак стенозов у детей — нарушение функции внешнего дыхания, которое колеблется от небольшого учащения ЧДД до шумного и свистящего дыхания. Чтобы облегчить состояние, ребенок присаживается на корточки, садится, наклонившись вперед с упором на руки. Родители замечают, что при вдохе втягиваются межреберные промежутки, над- и подключичные ямки. Одышка сохраняется даже в покое.
Симптомы сужения гортани включают изменение цвета кожи. Ребенок становится бледным, вокруг губ появляется синеватый оттенок. При прогрессировании стеноза наблюдается тотальный цианоз кожного покрова. Беспокоит повышенная потливость, все тело покрывается липким холодным потом. При тяжелом поражении возможно непроизвольное мочеиспускание или дефекация, судороги. При асфиксии ребенок задыхается, после чего теряет сознание.
Осложнения
Грозное последствие тяжелого гортанного стеноза — летальный исход от остановки дыхания и расстройств сердечной деятельности. При длительном сужении просвета воздухоносных путей у детей возникают симптомы хронической гипоксии, которая нарушает работу внутренних органов и головного мозга, провоцирует отставание в физическом и психическом развитии. Рубцовая деформация чревата потерей голоса и инвалидизацией ребенка.
Диагностика
При развернутой клинической картине стеноза детский ЛОР ставит диагноз без дополнительных методов обследования и сразу переходит к оказанию экстренной помощи. Диагностический поиск выполняется при легких и среднетяжелых формах стеноза либо после купирования асфиксии и стабилизации состояния ребенка. Для обследования применяются инструментальные и лабораторные методы:
- Ларингоскопия. Как скрининговая диагностика используется непрямая ларингоскопия, которая производится быстро и дает врачу информацию о наличии и характере стеноза. Для изучения анатомического строения гортани и определения уровня сужения показана прямая ларингоскопия.
- Рентгенография. На рентгенологическом снимке в боковой проекции визуализируется рубцовая ткань, что необходимо для диагностики хронического стеноза. Чтобы точно установить локализацию и степень распространенности стенотических изменений, назначается компьютерная томография гортани.
- МРТ гортани. Проводится при затруднениях в диагностическом поиске. Она позволяет детально осмотреть состояние мягких тканей дыхательных путей и окружающей клетчатки, что дает отоларингологу ценную информацию для уточнения этиологического фактора стеноза.
- Эндоскопия. Фиброларинготрахеоскопия требуется для детального осмотра внутреннего состояния гортани, нижележащих отделов дыхательной системы. Методика сочетает диагностические и лечебные функции, поскольку с ее помощью можно удалить инородные тела и наладить нормальное дыхание.
- Лабораторные анализы. При подозрении на инфекционную природу стеноза у детей рекомендована микробиологическая диагностика мазка из зева или мокроты. Больным в тяжелом состоянии необходим расширенный биохимический анализ крови, выявляющий симптомы метаболических и гипоксических расстройств.
Лечение стеноза гортани у детей
Консервативная терапия
При острых стенозах медикаментозные мероприятия имеют вспомогательный характер и включаются в комплекс неотложной помощи. Ребенку вводят кортикостероиды в возрастных дозировках, антихолинэргические средства. Для компенсации гипоксии после устранения стеноза проводится дыхание увлажненными кислородными смесями. После стабилизации самочувствия лечение подбирается по этиопатогенетическому принципу.
Легкие формы болезни подлежат амбулаторной терапии, при остальных рекомендована госпитализация. Если выявлены симптомы ларингита, назначаются нестероидные противовоспалительные препараты, антигистаминные средства. Для ликвидации вязкой мокроты, которая закупоривает просвет дыхательных путей, используют муколитики, щелочные ингаляции (для детей после 4-5 лет). При необходимости подбирается антибактериальная терапия.
Соответственно причине стеноза в стационаре могут применяться противовирусные, противомикробные, противогрибковые препараты. Когда симптомы вызваны нервно-мышечными нарушениями, показаны миорелаксанты. При интенсивном отеке эффективны адреномиметики в виде растворов и ингаляций, которые обладают мощным сосудосуживающим эффектом. Из физиотерапии выполняют УФО, электрофорез на область шеи.
Хирургическое лечение
При остром развитии тяжелого стеноза и асфиксии оперативное вмешательство производится как можно быстрее. В экстренных случаях показана коникотомия — рассечение гортани между хрящами для обеспечения поступления воздуха в дыхательные пути. У детей старше 8 лет проводится менее травматичная пункционная коникотомия, в ходе которой устанавливается катетер с иглой.
При хронических рубцовых стенозах хирургическая коррекция выполняется в плановом порядке. Чаще используются эндоскопические операции: баллонная дилатация, лазерная микрохирургия, вмешательство с помощью микродебридера. У детей также применяют оперативное лечение с наружным доступом: ларингопластику с использованием аутотрансплантата, резекцию гортани, латерофиксацию голосовых складок.
Реабилитация
Для успешного восстановления после хирургического лечения ребенку назначают щадящий режим. Наблюдение у ЛОР-врача проводится в течение 2-3 месяцев один раз в 2 недели. Специалисты советуют соблюдать голосовой режим (тихий разговор, избегание крика и громкого смеха), исключить горячие и острые блюда, чтобы не раздражать слизистую и не провоцировать симптомы удушья.
Прогноз и профилактика
При стенозах 1-2 стадии у врачей есть время для выявления причины патологии и ее устранения, поэтому прогноз благоприятный. В случае декомпенсации состояния и развития асфиксии существует высокий риск смерти, если вовремя не оказана медицинская помощь. Профилактика заболевания включает раннее лечение ОРВИ (в частности парагриппа), избегание травм, проведение иммуностимулирующих и общеукрепляющих мероприятий.
Источник
Обзор литературы
Приобретенные гортаннотрахеальные стенозы остаются одной из сложнейших проблем детской оториноларингологии. Это связано не только с трудностью и многоэтапностью восстановления просвета дыхательных путей, но и с сочетанным с дыхательным стенозом и длительным трахеальным канюленосительством развитием патологических изменений в других органах и системах организма. Такие изменения приводят к инвалидности и социальной неполноценности, что требует тесного взаимодействия специалистов нескольких педиатрических дисциплин, таких, как оториноларингология, анестезиология, реаниматология, хирургия, пульмонология, гастроэнтерология, генетика [5, 10, 13, 18].
Ведущей причиной формирования рубцовых стенозов гортани является продленная чрезгортанная назотрахеальная интубация, проводимая по поводу острого стенозирующего ларинготрахеобронхита, операций и иных экстремальных ситуаций, требующих реанимационных мероприятий и искусственной вентиляции легких [5, 7, 11, 13, 33]. Повреждение тканей гортани при проведении интубации возникает в случае превышения капиллярного давления. Это вызывает ишемию тканей с последующим развитием воспаления, отека, изъязвления слизистой оболочки и дальнейшим возникновением хондроперихондрита и некроза, что можно сравнить с развитием «гортанного пролежня» [14]. Кроме того, стенозы могут быть связаны со спортивной, бытовой, транспортной и медицинской травмами [2, 14, 34, 35].
При бактериологическом исследовании отделяемого из трахеи у детей, нуждающихся в восстановительном лечении по поводу рубцового стеноза гортани, отмечается полимикробная флора (до восьми типов микроорганизмов одновременно), в том числе сочетание как аэробной, так и анаэробной флоры [15]; при этом, характер микробной флоры у детей и взрослых различается. Чаще всего у детей инфицирование происходит Pseudomonas aeruginosa, Staphylococcus aureus, Acinetobacter и Haemophilus influenzae [31].
Рентгенографическое исследование, являющееся наиболее распространенным дополнительным методом диагностики [2, 44], в связи с малой контрастностью тканевых структур гортани не всегда дает объективную картину [42], а ультразвуковое исследование гортани к настоящему времени еще не получило широкого распространения [4]. «Золотым стандартом» диагностики рубцового стеноза гортани и трахеи являются прямая микроларингоскопия и трахеобронхоскопия с использованием операционного микроскопа и оптических трубок [13, 18, 23, 36]. Эти методы позволяют точно оценить протяженность и степень стеноза, его характер и локализацию; следует также иметь в виду, что у 1/5–1/2 пациентов возможны комбинированные поражения на различных уровнях дыхательных путей [18, 23].
В результате повреждения дыхательных путей могут формироваться различные виды обструкции. Повреждения гортани у новорожденных и детей младшего возраста часто (до 22% случаев) протекают с явлениями хондроперихондрита, лечение которого включает в себя противовоспалительную и гормональную терапию [9]. У детей младшего возраста эндоскопическое бужирование гортани в сочетании с противовоспалительным лечением в процессе формирования рубцовой ткани при ее незрелости и остаточных воспалительных процессах на ограниченном участке может оказаться эффективным. В то же время диффузный перихондрит хрящевого каркаса гортани и сформировавшийся рубец являются противопоказаниями к проведению бужирования [11].
Наиболее тяжелое осложнение чрезгортанной интубации трахеи и трахеостомии — это развитие рубцового стеноза. Рубцы могут локализоваться в различных отделах дыхательных путей — между черпаловидными хрящами, на уровне голосовых складок, в подскладковом отделе, в шейном и грудном отделах трахеи [14, 32]. По данным Э. А. Цветкова (1996), более чем у 70% больных детей рубцовый процесс занимает подголосовой отдел гортани и гортаннотрахеальное сочленение. Согласно исследованиям А. Д. Понкратенко, Е. К. Онуфриевой (1997), среди 183 детей с рубцовым стенозом гортани рубцы локализовались в голосовом отделе у 36 больных, в подскладковом — у 118, сочетанное поражение разных отделов гортани отмечено у 29 пациентов.
Хирургическое устранение рубцового стеноза возможно двумя принципиально разными доступами — через естественные пути или с рассечением гортани и трахеи. Эндоскопические хирургические вмешательства при рубцовых стенозах всегда предпочтительнее эндоларингеальных с наружным доступом [11, 29]. Прямая микроларингоскопия и эндоларингеальная микрохирургия, особенно с использованием лазерной техники, позволяет у значительной части больных устранить рубцовый стеноз гортани и гортаннотрахеального отдела с достаточно хорошим функциональным эффектом. Лазерные операции практически бескровны, отличаются малой травматичностью и вследствие этого не сопровождаются выраженными реактивными явлениями. Другим преимуществом лазерных операций по сравнению с операцией наружным доступом является интактность хрящевого остова, что способствует более быстрому заживлению и восстановлению просвета гортани, позволяя максимально сохранить голосовую функцию [13]. Особенности процессов репарации после лазерных операций дают возможность у большинства больных, в том числе у детей младшего (до трех лет) возраста, восстанавливать просвет дыхательных путей без дополнительного применения стентов [1, 9, 13], хотя в ряде случаев их приходится использовать для поддержания воссозданного просвета [6, 48]. Лазерная хирургия рубцовых стенозов эффективна также в случаях, когда предыдущие операции с применением других методик не дали хорошего результата [37]. Катамнестические наблюдения свидетельствуют о том, что воссозданный с помощью лазерной операции просвет дыхательных путей сохраняется с ростом гортани и обеспечивает нормальную дыхательную функцию [5].
Одним из главных критериев отбора больных для эндоскопической лазерной хирургии является протяженность рубца, которая не должна превышать 1,5-2 см [1, 7, 13, 25]. Лечение оказывается малоэффективным при вовлечении в рубцовый процесс хрящевого скелета [7]. Кроме того, необходимо учитывать фазу формирования стеноза. В тех случаях, когда имеются явления хондроперихондрита, вопрос о необходимости лазерной операции целесообразно отложить до ликвидации воспалительных явлений [9]. Предпочтительнее всего проводить операцию через год и более после травматического повреждения гортани и формирования стеноза, однако положительного результата удается достичь и при лечении детей в ближайшие сроки (до двух месяцев) после травмы дыхательных путей [12]. При анализе результатов повторных операций по поводу рубцового стеноза гортани отмечается определенная связь: при неэффективном первичном хирургическом вмешательстве в 50% наблюдений результат повторной операции оказывается аналогичным. Показанием к повторной операции является хотя бы минимальный эффект от предыдущей — небольшое увеличение просвета дыхательной трубки [13, 29]. При удовлетворительном результате первичной операции повторная в 80-90% наблюдений приводит к дальнейшему улучшению [12].
Показаниями к операции по устранению рубцового стеноза гортани наружным доступом служат протяженный (более 1-3 см) рубец, потеря хрящевой опоры выше или в области трахеостомы, отсутствие эффекта от эндоскопических операций, в том числе проводимых с помощью лазера [13, 26]. В литературе имеется скудная информация об оптимальных сроках подобных операций у детей. В то же время случаи возникновения различного рода осложнений и гибели детей при случайной деканюляции или закупорке трахеотомической трубки коркой наблюдаются достаточно часто и составляют до 4,6% [49]. Ларингостомия и длительное формирование просвета гортани с применением Т-образной трубки у детей затруднены, так как относительно толстые стенки трубки суживают и без того неширокий просвет дыхательных путей, вызывая развитие дисфагических явлений, бронхитов, аспирационных пневмоний, асфиксии [41]; применение Т-образных трубок эффективно только у 50% пациентов в возрасте до 10 лет по сравнению с 80% больных старше 10 лет [20]. Реконструктивные операции у детей младшего возраста имеют высокий статистически значимый риск неудачи, несмотря даже на меньшую тяжесть повреждения дыхательных путей, по сравнению со старшими детьми [50]. В то же время некоторые авторы рекомендуют оперировать детей раннего возраста как можно раньше в целях восстановления нормального речевого общения; при этом хронические трахеоканюляры, по сравнению с ранее не трахеотомированными больными, требуют более агрессивной тактики лечения; они имеют меньше шансов на успех операции, у таких больных чаще развиваются осложнения в послеоперационном периоде [25]. Среди новорожденных и детей младшего возраста предрасполагающими факторами к развитию осложнений являются вес меньше 4 кг и гестационный срок меньше 30 недель [28].
Для формирования стойкого просвета гортани осуществляются различные варианты редрессации печатки перстневидного хряща [8, 11, 46], ларинготрахеальной декомпрессии с расширением просвета дыхательных путей (в области как передней, так и задней стенки), в том числе путем пересадки аутохряща (реберного, ушной раковины, перегородки носа) [17, 19, 40], васкуляризированного трансплантата из тела подъязычной кости с грудинно-подъязычной мышцей [11, 24, 27] и других тканей. Наиболее частыми причинами неудач операций, проведенных наружным доступом, являются недостаточная предоперационная диагностика гортаннотрахеального стеноза, интраоперационные дефекты, ошибки, связанные с выбором типа и длины стента и длительностью его использования, склонность к развитию келлоидных рубцов, недостаточное послеоперационное наблюдение [16], а также такая сопутствующая патология, как ларингомаляция, трахеомаляция и пролапс черпаловидных хрящей [38]. В ряде случаев для успешной деканюляции требуется несколько повторных операций наружным доступом; лечение может затягиваться на десятки лет [22]. Противопоказаниями к операции наружным доступом являются незаконченный процесс рубцевания, тяжелые поражения ЦНС, заболевания легких, неизлеченное первичное заболевание, невозможность послеоперационного наблюдения и лечения [11, 25].
В последние годы появились сообщения об устранении обширных стенозов гортани и трахеи у детей путем резекции стенозированного участка с последующим наложением межтрахеального и гортаннотрахеального анастомозов [30, 39]. Показанием к операции является изолированный подскладковый или трахеальный стеноз, расположенный как минимум на 10 мм ниже голосовых складок; протяженность стеноза должна быть от 1 до 6 см [45]. При формировании анастомоза между гортанью и трахеей возникают значительные трудности из-за несоответствия размеров сшиваемых концов. Эти операции в основном используются при лечении взрослых больных; к настоящему времени отдаленные результаты такого лечения у детей еще не изучены (хотя эксперимент на кроликах показал адекватный рост дыхательных путей после резекции перстневидного хряща и первого кольца трахеи [47]), у них высок риск развития дигисценций в области анастомоза, повреждения возвратных нервов; кроме того, в случае неудачи операции дальнейшее лечение крайне затруднительно [18]. Даже незначительный отек тканей в месте анастомоза может вызывать у ребенка выраженный дыхательный стеноз, связанный с малым диаметром трахеи; при этом трахея ребенка менее толерантна к растяжению, чем у взрослого, в связи с чем резекция у ребенка возможна лишь на относительно меньшей, по сравнению со взрослым, части трахеи [21]. По мнению В. Г. Зенгера (2001), при циркулярной резекции трахеи и дополнительной мобилизации подъязычной кости происходит вмешательство в очень сложный механизм, обеспечивающий одну из важнейших функций гортани — защитную, так как возникает опасность проявления аспирационных осложнений. В случае возникновения осложнений необходимо дополнительное разобщение отрезков воздухопроводящих путей, т. е. выполнение трахеостомии и введение трахеальной канюли с раздувной манжеткой, что сводит на нет все преимущества столь сложной и небезопасной для больного операции. Поэтому возможность частичной резекции дыхательных путей с наложением анастомоза должна рассматриваться лишь в качестве крайнего варианта [3].
Несмотря на использование различных по технике операций, эффективность устранения рубцового стеноза гортани и деканюляции достигает, согласно наблюдениям различных авторов, 63–64 % [5, 11, 18, 43]. На эффективность лечения влияют степень сужения дыхательных путей и протяженность стеноза: если при стенозе гортани до 70% просвета удается деканюлировать до 100% детей, то при полной атрезии органа эффективность оперативного вмешательства снижается до 67% деканюлированных больных (в том числе и после повторных операций) [46]; кроме того, чем короче стенозированный участок, тем результативнее лечение [12]. По мнению B. Benjamin (1993), при сочетанном поражении складкового и подскладкового отделов гортани, особенно при их тотальной облитерации рубцовой тканью, реконструктивные операции достигают успеха приблизительно в 50% случаев.
Литература
- Богомильский М. Р., Гаращенко Т. И., Онуфриева Е. К. и др. Эндоскопическое применение хирургических лазеров при стойких обструктивных процессах в гортанной части глотки, гортани и трахее у детей // Вестник оторинолар. 1999. № 1. С. 39-41.
- Зенгер В. Г., Наседкин А. Н. Повреждения гортани и трахеи. М.: Медицина, 1991. 221 с.
- Зенгер В. Г. К вопросу о восстановлении просвета гортани после ее циркулярной резекции с последующей окклюзией и хроническим канюленосительством / Заболевания голосового аппарата и верхних дыхательных путей / Юбилейный сб. науч. трудов симпозиума, посвященного 10-летию Ассоциации фониатров и фонопедов, 24-27 мая 2001 г. (г. Владимир). Москва – Владимир, 2001. С. 193-196.
- Петухова Л. И., Солдатский Ю. Л., Быковский В. А., Романов Д. В. Ультразвуковые аспекты диагностики заболеваний гортани у детей младшего возраста // Эхография. 2000. Т. 1. № 3. С. 330-334.
- Понкратенко А. Д., Онуфриева Е. К. Отдаленные результаты эндоскопической СО2 -лазерной хирургии рубцовых стенозов гортани у детей // Вестник оторинолар. 1997. № 4. С. 16-19.
- Понкратенко А. Д., Солдатский Ю. Л., Нурмухаметов Р. Х. Применение стентов в СО2-лазерной эндоскопической хирургии рубцовых стенозов гортани у детей // Новости оториноларингологии и логопатологии. 1998. № 1. С. 80-83.
- Руин А. Г. Проблемы деканюляции у детей с хроническим трахеальным канюленосительством при рубцовых стенозах гортани и шейного отдела трахеи: Автореф. дис. … канд. мед. наук. М., 2000. 20 с.
- Савин А. Н. Ларингопластика с редрессацией задней стенки гортани при рубцовых и паралитических стенозах. Автореф. дис. … канд. мед. наук. СПб., 1997. 22 с.
- Солдатский Ю. Л., Понкратенко А. Д., Онуфриева Е. К. Лазерная хирургия постинтубационных стенозов гортани у детей младшего возраста // Лазерная медицина. 1999. Т. 3. № 2. C. 18-21.
- Фадеева И. А. Гортанно-кардиальные взаимодействия у детей // Новости оториноларингологии и логопатологии. 1998. № 1. С. 84-89.
- Цветков Э. А. Современные проблемы этиологии и лечения рубцовых стенозов гортани у детей // Новости оториноларингологии и логопатологии. 1996. № 3-4. С. 76-78.
- Чирешкин Д. Г., Зенгер В. Г., Онуфриева Е. К., Шустер А. М. Об оптимизации хирургического лечения детей с приобретенным рубцовым стенозом гортани и шейного отдела трахеи // Вестник оторинолар. 1991. № 6. С. 47-51.
- Чирешкин Д. Г. Хроническая обструкция гортанной части глотки, гортани и трахеи у детей. Этиология, клиника и методы устранения. М.: Рапид-Принт. 1994. 144 с.
- Benjamin B. Prolonged intubation injuries of the larynx: endoscopic diagnosis, classification, and management //Ann Otol Rhinol Laryngol. 1993.Vol. 102. № 4. Pt 2. Suppl. 160. 15 p.
- Brown O. E., Manning S. C. Microbial flora of the subglottis in intubated pediatric patients // Int. J. Pediatr Otorhinolaryngol. 1996. Vol. 35. № 2. P. 97-105.
- Choi S. S., Zalzal G. H. Pitfalls in laryngotracheal reconstruction // Arch. Otolaryngol. Head Neck. Surg. 1999. Vol. 125. № 6. P. 650-653.
- Cotton R. T., Myer C. M. 3d, O’Connor D. M., Smith M. E. Pediatric laryngotracheal reconstruction with cartilage grafts and endotracheal tube stenting: The single-stage approach // Laryngoscope. 1995. Vol. 105. № 8. Pt. 1. P. 818-821.
- Cotton R. T. Management of subglottic stenosis // Otolaryngol. Clin. Norht. Am. 2000. Vol. 33, № 1. P. 111-130.
- De Jong A. L., Park A. H., Raveh E., Schwartz M. R., Forte V. Comparsion of thyroid, auricular, and costal cartilage donor sites for laryngotracheal reconstruction in an animal model // Arch. Otolaryngol. Head. Neck. Surg. 2000. Vol. 126. № 1. P. 49-53.
- Gaissert H. A., Grillo H. C., Mathisen D. J., Wain J. C. Temporary and permanent restoration of airway continuity with the tracheal T tube // J. Thorac. Cardiovasc. Surg. 1994. Vol. 107. № 2. P. 600-606.
- Grillo H. C. Pediatric tracheal problems // Chest Surg Clin North Am. 1996. Vol. 6. № 4. P. 693-700.
- Gustafson L. M., Hartley B. E. J., Cotton R. T. Acquired total (grade 4) subglottic stenosis in children //Ann. Otol. Rhinol. Laryngol. 2001. Vol. 110. № 1. P. 16-19.
- Holinger L. D., Lusk R. P., Green C. G. Pediatric laryngology and bronchoesophagology. Philadelphia-New York: Lippincott-Raven, 1997. 402 p.
- Keghian J., Lawson G., Orban D., Remacle M. Composite hyoid-sternohyoid interposition graft in the surgical treatment of laryngotracheal stenosis // Eur. Arch. Oto-Rhino-Lar. 2000. Vol. 257. № 10. P. 542-547.
- Lesperance M. M., Zalzal G. H. Laryngotracheal stenosis in children // Eur Arch Otorhinolaryngol. 1998. Vol. 255. № 1. P. 12-17.
- McCaffrey T. V. Management of laryngotracheal stenosis on the basis of site and severity // Otolaryngol. Head. Neck. Surg. 1993. Vol. 109. № 3. Pt 1. P. 468-473.
- McGuirt W. F. Jr., Little J. P., Healy G. B. Anterior cricoid split. Use of hyoid as autologous grafting material // Arch. Otolaryngol. Head. Neck. Surg. 1997. Vol. 123. № 12. P. 1277-1280.
- McQueen C. T., Shapiro N. L., Leighton S., Guo X. G., Albert D. M. Single-stage laryngotracheal reconstruction. The Great Ormond experience and guidelines for patient selection // Arch. Otolaryngol. Head. Neck. Surg. 1999. Vol. 125. № 3. P. 320-322.
- Mehta A. C., Harris R. J., De Boer G. E. Endoscopic management of binign airway stenosis // Clin. Chest. Med. 1995. Vol. 16. № 3. P. 401-413.
- Monnier P., Lang F., Savary M. Partial cricotracheal resection for severe pediatric subglottic stenosis: update of the Lausanne experience // Ann Otol. Rhinol. Laryngol. 1998. Vol. 107. № 11, Pt. 1. P. 961-968.
- Morar P., Singh V., Jones A. S., Hughes J., van Saene R. Impact of tracheotomy on colonization and infection of lower airways in children requiring long-term ventilation: a prospective observational cohort study // Chest. 1998. Vol. 113. № 1. P. 77-85.
- Myer C. M.3d, Hartley B. E .J. Pediatric laryngotracheal surgery // Laryngoscope. 2000. Vol. 110. № 11. P. 1875-1883.
- Pereira K. D., Mitchell R. B., Younis R. T., Lazar R. H. Subglottic stenosis complicating cardiac surgery in children // Chest. 1997. Vol. 111. № 6. P. 1769-1772.
- Perkins J. A., Inglis A. F. Jr., Richardson M. A. Iatrogenic airway stenosis with reccurrent respiratory papillomatosis // Arch. Otolaryngol. Head. Neck. Surg. 1998. Vol. 124. № 3. P. 281-287.
- Randestad A., Lindholm C. E., Fabian P. Dimensions of the cricoid cartilage and the trachea // Laryngoscope. 2000. Vol. 110. № 11. P. 1957-1961.
- Richtsmeier W. J., Scher R. L. Telescopic laryngeal and pharyngeal surgery // Ann. Otol. Rhinol. Laryngol. 1997. Vol. 106. № 12. P. 995-1001.
- Rimell F. L., Dohar J. E. Endoscopic management of pediatric posterior glottic stenosis // Ann. Otol. Rhinol. Laryngol. 1998. Vol. 107. № 4. P. 285-290.
- Rutter M. J., Link D. T., Liu J. H., Cotton R. T. Laryngotracheal reconstruction and the hidden airway lesion // Laryngoscope. 2000. Vol. 110. № 11. P. 1871-1874.
- Rutter M. J., Hartley B. E. J., Cotton R. T. Cricotracheal resection in children // Arch. Otolaryngol. Head. Neck. Surg. 2001. Vol. 127. № 3. P. 289-292.
- Silva A. B., Lusk R. P., Muntz H. R. Update on the of auricular cartilage in laryngotracheal reconstruction // Ann. Otol. Rhinol. Laryngol. 2000. Vol. 109. № 4. P. 343-347.
- Stern Y., Willging P. J., Cotton R. T. Use of Montgomery T-tube in laryngotracheal reconstruction in children: is it safe? // Ann. Otol. Rhinol. Laryngol. 1998. Vol. 107. № 12. P. 1006-1009.
- Tostevin P. M., de Bruyn R., Hosni A., Evans J. N. The value of radiological investigations in pre-endoscopic assessment of children with stridor // J. Laryngol. Otol. 1995. Vol. 109. № 9. P. 844-848.
- Triglia J. M., Nicollas R., Roman S. Management of subglottic stenosis in infancy and childhood // Eur. Arch. Oto-Rhino-Lar. 2000. Vol. 257. № 7. P. 382-385.
- Walner D. L., Ouanounou S., Donnelly L. F., Cotton R. T. Utility of radiographs in the pediatric airway obstruction // Ann. Otol. Rhinol .Laryngol. 1999. Vol. 108. № 4. P. 378-383.
- Walner D. L., Stern Y., Cotton R.T. Margins of partial cricotracheal resection in children // Laryngoscope. 1999. Vol. 109. № 10. P. 1607-1610.
- Ward R. F., Gordon M., Rabkin D., April M. M. Modifications of airway reconstruction in children // Ann. Otol. Rhinol. Laryngol. 1998. Vol. 107. № 5. Pt 1. P. 365-369.
- Ward R. F., Triglia J. M. Airway growth after cricotracheal resection in a rabbit model and clinical application to the treatment of subglottic stenosis in children // Laryngoscope. 2000. Vol. 110. № 5. P. 835-844.
- Werkhaven J. A., Beste D. Diagnosis and management of pediatric laryngeal stenosis // Otolaryngol. Clin. North Am. 1995. Vol. 28. № 4. P. 797-808.
- Wetmore R. F., Marsh R. R., Thompson M. E., Tom L. W. C. Pediatric tracheotomy: a changing procedure? // Ann. Otol. Rhinol. Laryngol. 1999. Vol. 108. № 7. Pt 1. P. 695-699.
- Zalzal G. H., Choi S. S., Patel K. M. Ideal timing of pediatric laryngotracheal reconstruction // Arch. Otolaryngol. Head. Neck. Surg. 1997. Vol. 123. № 2. P. 206-208.
Источник