Лечение лучевой терапией рака гортани
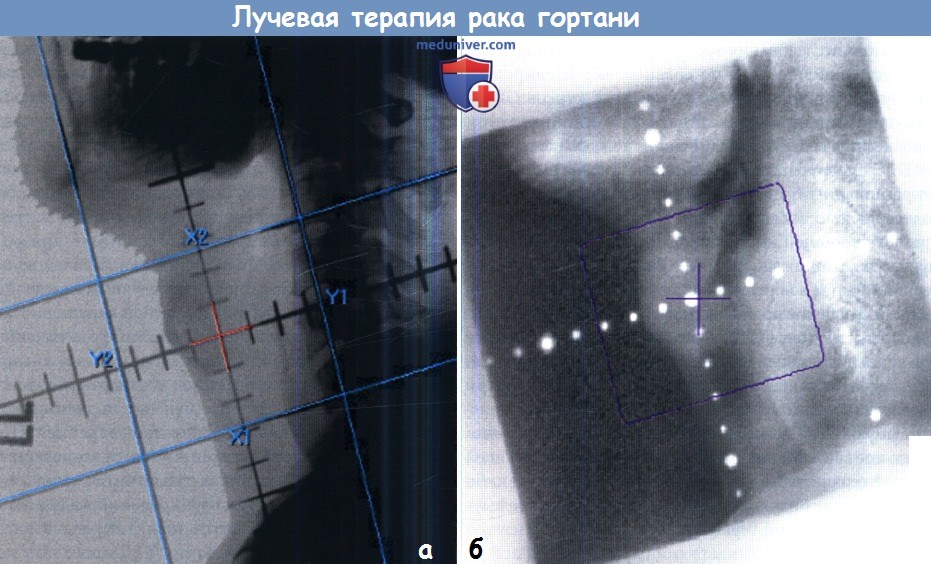
Методы лучевой терапии при раке гортани
а) Лучевая терапия складочного отдела гортани. Новообразования голосовых складок ранних стадий имеют низкую метастатическую активность, поэтому зачастую они могут быть успешно устранены использованием лишь одного метода лечения. На ранних стадиях применяется либо хирургическое, либо лучевое лечение; распространенные формы рака требуют комбинации хирургического, лучевого и химиотерапевтического воздействия.
При распространенных опухолях мультидисциплинарный подход позволяет достичь максимального излечения, сохранить функцию пораженного органа, ограничить регионарное распространение, а также гораздо проще приспособиться к сопутствующим заболеваниями пациента и его индивидуальным предпочтениям.
На ранних стадиях заболевания при помощи лучевой терапии без ее сочетания с химиотерапией можно добиться и контроля опухолевого роста, и сохранения функции гортани. На настоящий момент чаще всего используются простые односторонние латеральные поля излучения в дозе 63-65 Гр за 28-29 сеансов в течение пяти с половиной недель.
Избирательное облучение гортани, не затрагивающее регионарные лимфоузлы, позволяет минимизировать повреждение крупных слюнных желез, нижней челюсти, ротоглотки и полости рта. Важны длительность курса и общая доза облучения. Оптимальная продолжительность курса составляет менее шести недель. У пациентов с опухолью стадии Т2 и с нарушением подвижности голосовой складки улучшить контроль над местным ростом опухолевой ткани можно посредством гиперфракционированного облучения (однако возрастает и общая токсичность).
Опухоли стадии Т2, поражающие надскладочный отдел гортани, могут потребовать селективного воздействия на лимфоузлы шеи. Подавления опухолевого роста можно добиться более чем в 90% случаев на стадии Т1, и более чем в 80% на стадии Т2.
При распространенном раке гортани стандартом лечения остается тотальная ларингэктомия с последующей лучевой терапией. Министерством по делам ветеранов США было организовано исследование эффективности лечения больных с раком гортани (Department of Veterans Affairs (VA) Laryngeal Cancer Study). Согласно его результатам, добиться сохранения функции гортани удалось у 2/3 пациентов, которым проводилась индукционная терапия тремя курсами 5-фторурацила/цисплатина с последующей лучевой терапией.

Рак гортани ранней стадии, локализующийся в области голосовой щели.
Двухмерная техника с использованием противоположных латеральных полей. Верхняя и нижняя границы устанавливаются с учетом подвижности гортани, которая будет отмечаться во время лечения.
Обратите внимание на то, что лимфоузлы не облучаются.
В качестве контрольной группы были выбраны пациенты, которым выполнялась тотальная ларингэктомия с последующей послеоперационной лучевой терапией. Разницы в выживаемости между двумя группами получено не было. Последующее крупное рандомизированное международное исследование сравнило курс лечения министерства по делам ветеранов (VA) с химиолучевой терапией и с изолированной лучевой терапией. Согласно его результатам, химиолучевая терапия позволяет добиться большей вероятности сохранения гортани, чем курс министерства (с 75% до 88%), поэтому на данный момент химиолучевая терапия является стандартом лечения.
Статистически значимой разницы в выживаемости между тремя группами получено не было (из-за высокой частоты выполнения ларингэктомий в качестве «терапии отчаяния»).
Следовательно, для пациентов с хорошим функциональным статусом гортани рекомендуется проведение семинедельной лучевой терапии с общей дозой в 70 Гр в сочетании с тремя курсами цисплатина в высоких дозах (100 мг/м2). В качестве альтернативы может использоваться индукционная трехкомпонентная (TPF) химиотерапия с последующей лучевой терапией, данная схема также позволяет добиваться высокой частоты сохранения гортани. Две эти схемы лечения рака гортани не сравнивались в рандомизированных исследованиях.
У ослабленных пациентов, которые не могут перенести стандартный курс химиотерапии, может использоваться либо изолированная лучевая терапия, либо лучевая терапия в сочетании с биологической терапией (моноклональные антитела против ЭФР).
У пациентов, получающих изолированную лучевую терапию, можно использовать либо курс модифицированного фракционного облучения (либо с гиперфракционированием, либо ускоренным курсом), поскольку превосходство двух этих схем над стандартной однодневной схемой облучения была продемонстрирована в исследовании RTOG 90-03.
Из названных выше исследований исключались пациенты, у которых опухоль прорастала в хрящи гортани и/или окружающие мягкие ткани. В данной группе стандартом лечения является ларингэктомия с последующей адъювантной лучевой терапией и, возможно, химиотерапией.
б) Лучевая терапия надскладочного отдела гортани. Пациенты с опухолями надскладочного отдела нуждаются в терапии лимфоузлов шеи даже на ранних стадиях заболевания, поскольку риск их вовлечения крайне высок. Первичная опухоль может распространяться в окологортанное пространство, вызывая фиксацию голосовых складок; в преднадгортанное пространство с поражением корня языка; через щитовидный хрящ проникать в мягкие ткани шеи; при латеральном распространении возможно поражение горганоглотки.
Опухоли Т1/Т2 надскладочного отдела требуют лечения первичного очага и лимфатических узлов уровней II—IV. Как и при раннем раке голосовых складок, в данном случае можно использовать какой-то один метод лечения. При лучевой терапии используют дозу 66-70 Гр для первичного очага и 50-54 Гр для элективного лечения лимфоузлов шеи. При использовании традиционных схем возможно избежать облучения околоушных слюнных желез и верхнего констриктора глотки.
При распространенных опухолях у пациентов с исходным хорошим функциональным статусом гортани и удовлетворительным общим состоянием используется химиолучевая терапия. При значительном нарушении функции гортани и/или распространении опухоли за пределы органа прибегают к ларингэктомии с последующей адъювантной лучевой терапией.
в) Лучевая терапия подскладочного отдела гортани. Опухоли, расположенные под голосовыми складками, встречаются крайне редко. Визуализировать их сложно даже с использованием эндоскопического оборудования, часто для этого требуется общая анестезия. Из-за своего скрытого расположения данные новообразования часто диагностируются уже на поздних стадиях, когда опухоль распространяется в трахею и мягкие ткани шеи.
Они способны метастазировать в нижние шейные лимфоузлы и верхние лимфоузлы средостения. Комбинированное хирургическое лечение показано при опухолях Т4 стадии, в остальных случаях прибегают к лучевой терапии, захватывающей и первичный очаг опухоли, и пути лимфатического оттока.
– Также рекомендуем “Осложнения лучевой терапии головы, шеи и ее побочные эффекты”
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Оглавление темы “Болезни полости рта и глотки”:
- Методы лучевой терапии при раке гортани
- Осложнения лучевой терапии головы, шеи и ее побочные эффекты
- Особенности анатомии полости рта
- Причины и патогенез рака полости рта
- Стадии рака полости рта и классификация по TNM
- Жалобы при раке полости рта и его диагностика
- Методы лечения рака полости рта и его осложнения
- Признаки доброкачественного образования полости рта
- Особенности анатомии глотки и пищевода
- Бактерии как причина боли в горле – фарингита
Источник
При подтвержденном диагнозе «рак гортани» лечение назначается с учетом стадии заболевания, местоположения и агрессивности опухоли, а также общего состояния здоровья пациента.
Для составления оптимальной схемы больной может быть отправлен на консультацию к различным специалистам – радиохирургу, онкохирургу, химиотерапевту и радиотерапевту.
Если новообразование с низкой степенью злокачественности обнаруживают рано, объем терапии минимален, а ее эффективность высока. Как правило, у таких больных удается добиться полной ремиссии, и они на долгие годы забывают о своих проблемах. В запущенных случаях объем лечения при раке гортани увеличивается, а прогноз ухудшается.
Стадии и степень злокачественности рака гортани
Начало болезни обычно протекает бессимптомно вне зависимости от местоположения опухоли, которая, как правило, развивается из небольшого доброкачественного узла слизистой оболочки – полипа. Если такой рак выявляется при проведении ларингоскопии, он может быть полностью удален прямо во время диагностического исследования.
На 2 стадии новообразование все еще остается в пределах слизистой, но значительно увеличивается в размерах. Если оно расположено в области голосовых связок, именно на этом этапе появляются первые симптомы.
По мере развития болезни опухоль прорастает в окружающие ткани и органы, злокачественные клетки обнаруживаются в близлежащих лимфоузлах.
На 4 стадии рака гортани лечение направлено на уменьшение первичного очага, устранение отдаленных метастазов и облегчение общего состояние пациента.
В то время как стадийность используется для определения распространенность процесса, степень злокачественности раковых клеток позволяет прогнозировать скорость роста опухоли и появления метастазов, а также эффективность лечения.
Принято выделять 3 степени злокачественности, которые устанавливаются по результатам биопсии:
- 1 степень характеризуется наличием атипичных клеток, мало отличающихся о нормальной ткани слизистой оболочки. Такая опухоль называется высокодифференцированной, она медленно растет и хорошо поддается лечению.
- Рак 2 степени более агрессивен, злокачественные клетки существенно отличаются от клеток ткани, из которой образовалось опухоль. Новообразование умеренно быстро увеличивается в размерах и хуже поддается лечению. В данном случае даже на ранней стадии обычно назначается комплексная терапия.
- Лечение рака гортани 3 степени осложнено его быстрым ростом и ранним появлением метастаз. При исследовании тканей такого очага обнаруживаются низкодифференцированные клетки, которые совсем не похожи на нормальные.
Основные методы лечения рака гортани
Составляя схему лечения рака гортани, лечащий врач выбирает наиболее эффективные и наименее травмирующие методы, тщательно взвешивая все «за» и «против».
Учитывая физиологические особенности данной части дыхательной системы, выполнение традиционной операции связано с высоким риском развития осложнений. Благодаря появлению новых прогрессивных технологий, врачи получили возможность отказаться от хирургического вмешательства при необходимости удаления локальных очагов размером до 5-6 см.
Лечение рака гортани Киберножом
Разрушение ракового узла с помощью радиохирургической установки Кибернож относится к радикальным методам, так как его результаты сопоставимы с результатами обычной операции. Радиохирургические облучение не только высокоэффективно, бескровно и безболезненно, но и в абсолютном большинстве случаев позволяет сохранить функциональность голосового аппарата, естественный характер дыхания и проглатывания пищи.
Как правило, после удаления Киберножом высокодифференцированных опухолей не требуется использование других методов. Если же установка применяется для лечения рака гортани 3 степени, радиохирургия может дополняться химиотерапией и/или тагретной терапией.
Дистанционная и контактная лучевая терапия (ЛТ)
В начале заболевания данные методы могут быть выбраны в качестве моно-лечения. Если рак обнаружен на продвинутой стадии и/или если при биопсии определена высокая степень злокачественности опухолевых клеток, ЛТ дополняется химиотерапией. Кроме того, лучевая терапия достаточно часто комбинируется с хирургией.
Хирургия
Анатомические особенности гортани обуславливают сложность выполнения классической хирургической операции. Наименее травмирующим методом является иссечение опухолевого узла во время эндоскопии с помощью лазера или специального хирургического инструмента. Однако эта малоинвазивная щадящая процедура выполняется только на ранней стадии заболевания.
В последние годы в Российской Федерации отмечается тенденция к стойкому и быстрому росту заболеваемости раком гортани. За последние 10 лет этот показатель увеличился на 20%. При этом более половины случаев диагнозов устанавливается на продвинутых стадиях. В этих случаях обычно показана ларингоэктомия.
- Операция по удалению голосового аппарата. Пораженный опухолью голосовой аппарат может быть удален полностью или частично. При полном удалении человек теряет способность дышать и говорить естественным образом, поэтому в процессе такой операции формируется стома – искусственное отверстие для дыхания. Впоследствии с помощью различных способов восстанавливается функция речи.
В последние годы в Российской Федерации отмечается тенденция к стойкому и быстрому росту заболеваемости раком гортани. За последние 10 лет этот показатель увеличился на 20%. При этом более половины случаев диагнозов устанавливается на продвинутых стадиях. В этих случаях обычно показана ларингоэктомия.
- Удаление лимфоузлов (шейная диссекция). На поздних стадиях больному показано хирургическое удаление пораженных раком шейных лимфоузлов.
Химиотерапия (ХТ)
Химиолечение входит в стандартные схемы терапии на поздних стадиях. Назначение некоторых видов ХТ перед курсом ЛТ (неоадъювантная химиотерапия) увеличивает эффективность облучения за счет повышения чувствительности раковых клеток к действию радиации.
Таргетная терапия
Таргетная или целевая терапия обычно назначается в комплексе с ХТ и ЛТ. Для этих целей используется препарат Цетуксимаб, обладающий целенаправленным угнетающим действием на клетки опухоли.
Последствия лечения
Помимо осложнений, проявляющихся физиологическими нарушениями, после хирургической операции возможно развитие инфекций и кровотечений.
Лечение Киберножом, как правило, проходит без каких-либо нежелательных последствий.
Комплексная терапия с использованием химиопрепаратов и облучения повышает интенсивность побочных эффектов каждого из методов, что учитывается онкологом при планировании курсов ХТ и ЛТ.
Восстановление после лечения
Полное восстановление после лечения Киберножом обычно происходит в течение нескольких часов или дней. Нахождение в клинике при этом не требуется.
После классической операции больного оставляют в больнице под наблюдением врача, при необходимости обучая заново глотать, есть и говорить, ухаживать за стомой.
Если вам требуется второе мнение для уточнения диагноза или плана лечения, отправьте нам заявку и документы для консультации, или запишитесь на очную консультацию по телефону.
+7 499 490-24-13
Экспертное мнение
Ласков Михаил Савельевич
Научная степень: кандидат медицинских наук
Специализация: онколог, гематолог, химиотерапевт
Должность: главврач
Место работы: «Клиника амбулаторной онкологии и гематологии»
Город: Москва
Работал в ведущих онкоцентрах США и Великобритании. Стажировался по медицинскому менеджменту в Канаде, Германии, Сингапуре. Автор ряда публикаций, участвует в научных программах в качестве главного исследователя. Приглашенный эксперт тематических радио- и теле-эфиров на ТВ-каналах «Дождь», «Мир», «РБК» и др., радио «Свобода», «Эхо Москвы», «Маяк» и др. Публикует статьи и дает интервью журналистам популярных изданий «АИФ», «Женское здоровье» и др.
Источник
Цели лечения рака гортани
Особенность планирования лечения рака гортани состоит в том, что необходимо не только излечить больного, но и восстановить голосовую, дыхательную и защитную функции гортани. На ранних стадиях заболевания полного выздоровления можно добиться с помощью лучевой терапии, органосохраняющих операций или сочетания этих методов.
Не следует догматически подходить к выполнению первоначального плана лечения. В процессе лучевой терапии выявляют одну из наиболее существенных характеристик опухоли – радиочувствительность. В зависимости от её выраженности производят коррекцию первоначального плана лечения.
Планирование лечения необходимо проводить на консилиумах хирургов, лучевых терапевтов, химиотерапевтов. При необходимости для участия в консилиуме приглашают эндоскопистов, рентгенологов и патоморфологов. Для обсуждения плана лечения необходимо располагать информацией о локализации опухоли в гортани, её границах, распространении на соседние отделы, преднадгортанниковое и околоскладочное пространство, форме роста, особенностях гистологического строения и морфологической дифференцировке. В процессе лечения к этим критериям добавляют информацию о радиочувствительности опухоли, оценивая степень уменьшения новообразования в процессе лучевой терапии. При биопсии после предоперационной лучевой терапии или микроскопического исследования после хирургического вмешательства правильность оценки этого критерия может быть проконтролирована при определении степени лучевого патоморфоза опухоли.
Немедикаментозное лечение рака гортани
Рак среднего отдела гортани Т1-Т2 обладает высокой радиочувствительностью, поэтому лечение начинают с лучевой терапии. Лучевое лечение в предоперационном периоде (доза облучения 35-40 Гр) не ухудшает заживление тканей, если после него выполняют операцию. В тех случаях, когда степень уменьшения опухоли больше 50% её первоначального объема, а остаток небольшой, через 2 нед продолжают лучевую терапию до достижения терапевтической дозы (60-65 Гр). С помощью морфологических исследований было показано, что через 3-4 нед после предоперационной дозы лучевой терапии опухоль начинает восстанавливаться за счёт радиорезистентных клеток: тем самым нивелируется предоперационный эффект лучевой терапии. В связи с этим интервал между этапами лечения не должен превышать 2 нед.
Следует отметить, что хирургическое вмешательство, выполняемое после полной дозы лучевой терапии, чревато опасностью развития послеоперационных осложнений, приводящих к образованию свищей, аррозий магистральных сосудов, существенно пролонгирующих послеоперационный период и затрудняющих его ведение.
При лечении рака голосовых складок Т1-Т2 лучевую терапию проводят с двух встречных полей под углом 90°: высота поля составляет 8 см, ширина – 6 см. При наличии регионарных метастазов можно рекомендовать поля, направленные сзади наперёд под углом 110°.
Вместо методик классического фракционирования дозы (по 2 Гр 5 раз в неделю)
В настоящее время применяют более эффективную методику дробления дозы на 3,3 Гр (по 1,65 Гр с каждого поля) 3 раза а неделю. Используя эту методику, можно за 10 лечебных сеансов в течение 22 дней поднести к опухоли дозу 33 Гр, эквивалентную по эффективности 40 Гp. При продолжении лучевой терапии по радикальной программе на 2-м этапе подводят к опухоли еще 25Гр. При этом используют классическое фракционирование дозы по 2 Гр 5 раз в неделю как более щадящее. Это позволяет избежать повреждении хрящей и развития хондроперихондрита.
Помимо лучевой терапии, проводимой в обычных условиях (в воздухе), разработан метод лучевой терапии в условиях гипербарической оксигенации. Преимуществами этого метода при предоперационном облучении считают усиление лучевого повреждения опухоли, уменьшение лучевого повреждения нормальных тканей, включенных в объём облучения, снижение частоты лучевых эпителиитов.
Использование гипербарической оксигенации позволило снизить при предоперационном облучении суммарную очаговую дозу до 23,1 Гр (7 сеансов по 3,3 Гр}, что эквивалентно 30 Гр при классическом фракционировании в тех случаях, когда изначально планируют комбинированное лечение с выполнением резекции гортани. Морфологическое изучение лучевого патоморфоза показало, что III степень патоморфоза у этих больных была в 2 раза выше, чем после подведения 33 Гр в воздухе. Подобные наблюдения послужили основанием для расширения показаний к самостоятельной лучевой терапии в условиях гипербарической оксигенации по радикальной программе.
При раке вестибулярного отдела гортани Т1-Т2 лечение следует начинать с лучевой терапии. Верхнюю границу поля облучения поднимают выше горизонтальной ветви нижней челюсти на 1,5-2 см. Методика фракционирования дозы и уровень суммарных очаговых доз при предоперационной лучевой терапии и облучении по радикальной программе для всех отделов гортани идентичны. Если после лучевой терапии в предоперационной дозе (40 Гр) опухоль уменьшается незначително (менее чем на 50%), то выполняют горизонтальную резекцию гортани.
Лечение рака вестибулярного отдела гортани ТЗ-Т4 начинают с химиотерапии. После 2 курсов химиотерапии проводят лучевую терапию в предоперационной дозе.
Окончательную тактику лечения определяют после подведения к опухоли дозы облучения 40 Гр. Больному выполняют резекцию гортани, если остаточная опухоль имеет небольшие размеры, и ларингэктомию при больших размерах опухоли, локализующиеся в области передней комиссуры, подкомиссуральной области, гортанного желудочка, черпаловидного хряща обычно радиорезистентны. Обнаружение поражения этих отделов гортани считают веским аргументом и пользу операции.
При раке подголосового отдела гортани ТТ-Т2 лечение также начинают с лучевой терапии. Её результаты оценивают после предоперационной дозы облучения 40 Гр. При уменьшении опухоли менее чем на 50% выполняют хирургическое вмешательство.
Зоны регионарного метастазирования включают в поле облучения при пред- или послеоперационной лучевой терапии по поводу рака гортани.
Наличие трахеостомы не является препятствием к проведению лучевой терапии: её включают в поле облучения.
Медикаментозное лечение рака гортани
Химиотерапию проводят больным распространённым раком надголосового отдела гортани (поражение корня языка, гортаноглотки, мягких тканей шеи). При раке подголосового и голосового отделов гортани химиотерапия малоэффективна.
Неоадъювантная химиотерапии состоит из 2 идентичных курсов с перерывами в 1 день между ними. Каждый блок включает:
- 1-й день. Циспластин в дозе 75 мг/м2 на фоне гипергидратации и форсированного диуреза.
- на 2-5-е сутки фторурацил в дозе 750 мг/м2.
Хирургическое лечение рака гортани
При выявлении радиорезистентности рака среднего отдела Т1-Т2 на 2-м этапе лечения после предоперационной лучевой терапии в дозе 40 Гр (в воздухе) выполняют органосохраняющую операцию. При раке голосового отдела гортани, если опухоль не распространяется на переднюю комиссуру и черпаловидный хрящ, выполняют боковую резекцию гортани. Если опухоль распространяется на переднюю комиссуру, производят переднебоковую резекцию . Следует отметить, что хирургический метод (резекция гортани) в качестве самостоятельного даёт сопоставимые результаты. Однако в этом случае исключена возможность излечения больного без операции с помощью лучевой терапии, при которой можно сохранить хорошее качество голоса.
При раке среднего отдела гортани ТЗ-Т4 на 1-м этапе проводят химиолучевое или лучевое лечение, на заключительном-ларингэктомию. В последние годы разработаны методики органосохраняющих операций операций при раке ТЗ, однако их выполняют по строгим показаниям. Излечение рака ТЗ с помощью лучевой терапии возможно только у 5-20% больных.
Разработана методика резекции гортани при ТЗ с эндопротезированием.
Показания к операции:
- поражение с одной стороны с переходом на переднюю комиссуру и другую сторону более чем на 1/3 при сохранении черпаловидных хрящей;
- поражение трёх отделов гортани с одной стороны с инфильтрацией подголосового отдела, требующее резекции перстневидного хряща.
Во избежание рубцового сужения гортани её просвет формируют на трубчатом протезе, изготовленном на основе винилпирролидона и акрилатон, пропитанных антисептиком, или из медицинского силикона. Через 3-4 нед после фор мирования каркаса просвета резецированной гортани протез удаляют через рот.
При раковой опухоли подголосового отдела гортани ТЗ-Т4 предоперационную лучевую терапию не проводят, т.к. у больных выражен стеноз просвета гортани до начала лечения или велика опасность его развития в процессе лучевой терапии Лечение начинают с ларингэктомии с 5-6 кольцами трахеи. Лучевую терапию проводят в послеоперационном периоде.
Основным методом лечения рецидивов рака гортани считают хирургического вмешательство. В зависимости от степени распространения опухоли, формы роста, морфологической дифференцировки планируют объём операции (от резекции до ларингэктомии).
Превентивные операции (при отсутствии пальпируемых и определяемых при УЗИ метастазов) выполняют при глубоком эндофитном росте опухоли с разрушением хрящей гортани, при распространении опухолей на гортаноглотку, щитовидную железу и трахею.
При наличии регионарных метастазов выполняют фасциально-футлярное иссечение лимфатических узлов и клетчатки шеи. При прорастании опухоли во внутреннюю ярёмную вену или грудино-ключично-сосцевидную мышцу резецируют эти анатомические структуры (операция Крайля). При обнаружении у больного раком гортани единичных метастазов в лёгких и печени решают вопрос о возможности их удаления.
Источник