Ларингэктомия при раке гортани
Методы открытых операций при раке гортаниИспользование открытых хирургических доступов в лечении злокачественных новообразований надсвязочного и связочного отделов гортани проверено долгими годами практики, с их помощью возможно добиваться отличных онкологических результатов. Среди открытых методов удаления новообразований выделяют, в порядке возрастания сложности: ларингофиссура с хордэкто-мией и последующей реконструкцией, вертикальная частичная ларингэктомия, надскдалочная горизонтальная ларингэктомия, надперстневидная ларингэктомия, тотальная ларингэктомия. Все варианты вмешательств, при которых гортань не удаляется полностью, называют органосохраняющими. Хордэктомия с последующей реконструкцией проводится пациентам с опухолью Т1, которым по каким-то причинам невозможно выполнение эндоскопической операции. У некоторых пациентов (например, с ретрогнатией, тризмом, лучевой терапией в анамнезе) визуализация передней комиссуры затруднена, поэтому удалить опухоль эндоскопически невозможно. Хордкэтомия с реконструкцией не рекомендуются пациентам, у которых опухоль прорастает на противоположную голосовую складку. Чаще всего необходима трахеотомия. При простой хордкэтомии приемлемым вариантом реконструкции является простое заживление вторичным натяжением, впоследствии, если это требуется, выполняется аугментационная медиализация. Также описаны методы интраоперационной реконструкции, когда новая голосовая складка формируется из подподъязычных мышц. В большинстве случаев у пациентов, которым была проведена хордэктомия с ларингофиссурой, функции речи и глотания сохраняются, хотя чаще всего голос становится слабым.
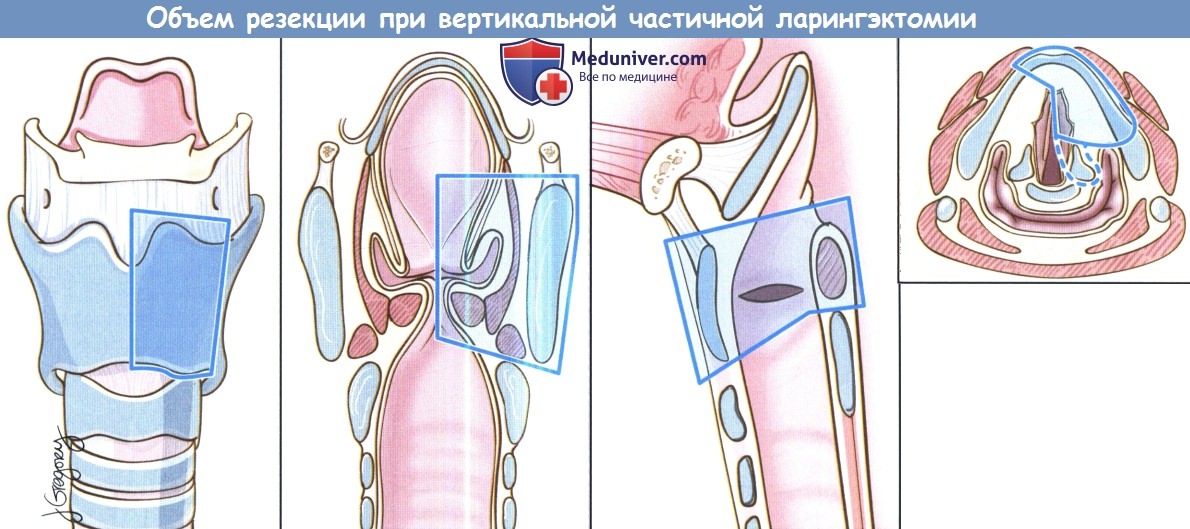
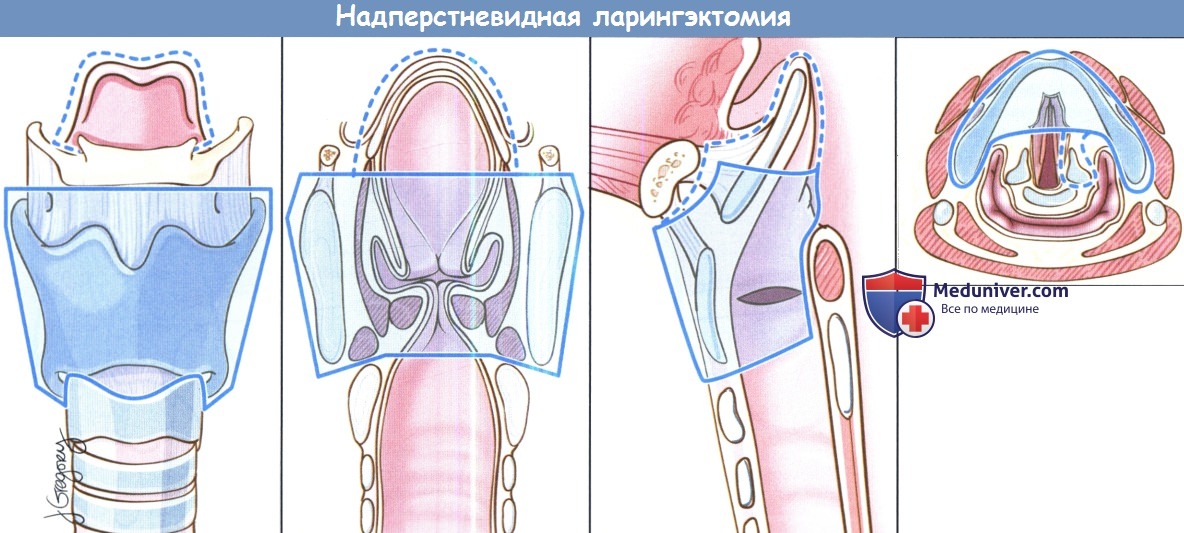
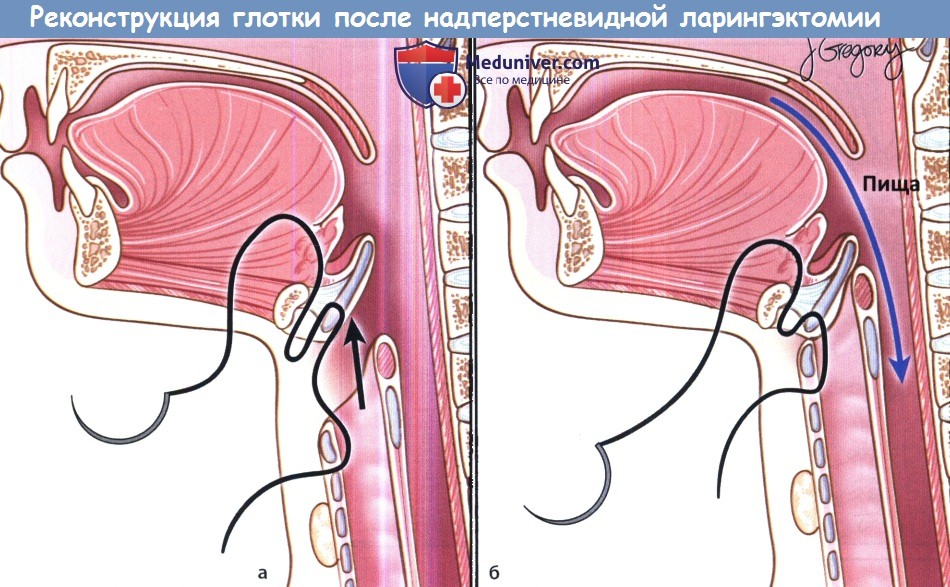
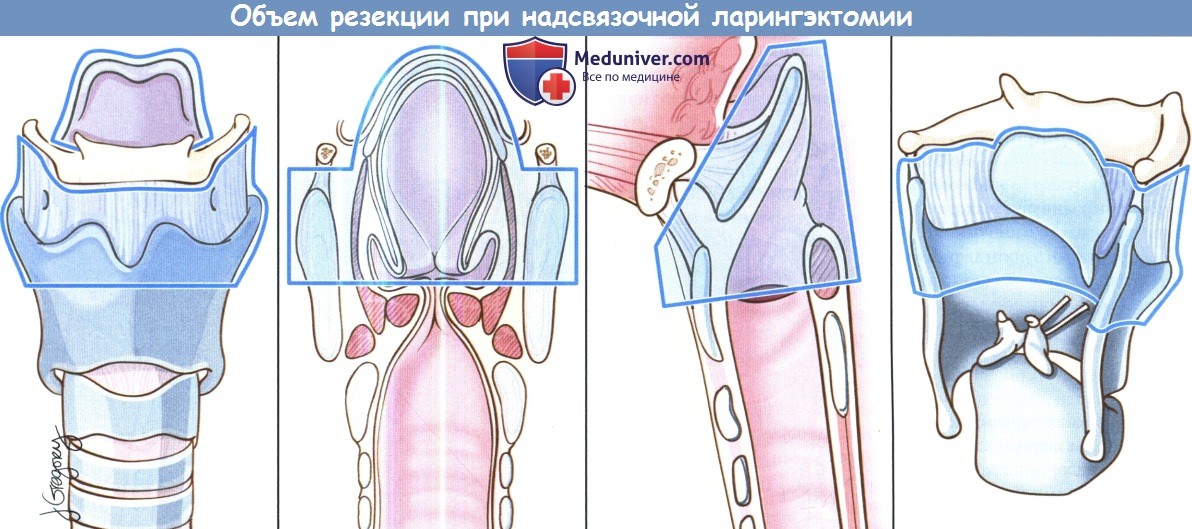
Вертикальная частичная ларингэктомия выполняется при опухолях Т1 и некоторых Т2. Чаще всего требуется трахеотомия. К противопоказаниям относится наличие опухоли Т3 без фиксации перстнечерпаловидного сустава, т.к. в данном случае предпочтительнее надперстневидная ларингэктомия. Выполняется ларингофиссура, локализация разреза для тиреотомии зависит от расположения опухоли, предварительно оцениваемого при помощи эндоскопии. При стандартной вертикальной частичной ларингэктомии голосовая складка удаляется от передней комиссуры до голосового отростка черпаловидного хряща сзади, вместе с внутренними мышцами гортани. Было описано множество «расширений» доступа, в том числе фронтолатеральная вертикальная гемиларингэктомия, заднелатеральная вертикальная гемиларингэктомия, расширенная вертикальная гемиларингэктомия. Как и при простой хордэктомии, описано множество вариантов реконструкции с целью восстановления голосовой функции. Открытая надскладочная ларингэктомия выполняется при опухолях Т1 и Т2, локализующихся в надсвязочном отделе гортани. Успешность лечения при опухолях Т1 составляет более 90%. Противопоказания включают распространение опухоли до уровня голосовой щели, инвазию в перстневидный или щитовидный хрящи, инвазию в корень языка более, чем на 1 см от желобовидных сосочков, поражение глубоких мышц языка или преднагортанникового пространства. При стандартной надскладочной ларингэктомии сохраняются обе голосовые складки, оба черпаловидных хряща, корень языка и подъязычная кость. При инвазии опухоли в преднагортанниковое пространство необходимо удаление подъязычной кости, которую в противном случае можно оставить нетронутой. При резекции щитовидной кости особенно важно сохранить верхний гортанный сосудисто-нервный пучок (также об этом необходимо помнить при надперстневидной ларингэктомии). Методы реконструкции те же, что и при надперстневидной ларингэктомии. Самый широкий спектр возможностей обеспечивает надперстневидная ларингэктомия, поскольку она может использоваться при опухолях Т1,Т2,Т3 и некоторых Т4 стадий, как при надскладочной, так складочной локализации. Выполнение надперстневидной ларингэктомии возможно и при снижении подвижности или фиксации голосовых складок, поражении гортанных желудочков или передней комиссуры, ограниченной эрозии щитовидного хряща без экстраларингеального распространения. В большинстве крупных исследований удавалось добиться высоких уровней пятилетней выживаемости и подавления местно-регионарного опухолевого роста. Противопоказаниями к надперстне-видной ларингэктомии являются фиксация перстнечерпаловидного сустава, поражение наружных мышц гортани, поражение возвратного гортанного нерва, распространение в подскладочное пространство более чем на 1 см, инвазия в перстневидный хрящ, заднюю комиссуру, экстраларингеальный рост, поражение надхрящницы наружной поверхности щитовидного хряща. Все ткани удаляются единым блоком. Резекция включает обе истинные голосовые складки, обе ложные голосовые складки, оба окологолосовых пространства, весь щитовидный хрящ, в некоторых случаях надгортанник, иногда один или оба перстневидных хряща. При разделении перстнечерпаловидных суставов крайне важно сохранить возвратные гортанные нервы. Как уже упоминалось выше, для сохранения в послеоперационном периоде нормального глотания крайне важно оставить нетронутыми верхние гортанные сосуды и нерв. Для реконструкции подъязычную кость, корень языка, в некоторых случаях и надгортанник, подшивают к перстневидному хрящу тремя симметричными подслизистыми швами викрилом 1-0.
Осложнения всех органосохраняющих операций сходны. Аспирация и дисфагия обычно встречаются лишь в раннем послеоперационном периоде, но у некоторых пациентов они сохраняются в течение длительного времени, требуя чрескожной гастростомии. Возможно формирование глоточно-кожных фистул, но риск ниже, чем при полной ларингэктомии. При выполнении органосохраняющих открытых методов, например, надперстневидной ларингэктомии, крайне важно, чтобы заново сформированная гортань была отделена от трахеостомы. Невозможность деканулировать пациента в послеоперационном периоде связана либо с повреждением возвратных гортанных нервов, либо с сужением просвета дыхательных путей из-за некачественно выполненной реконструкции. Наконец, при тотальной (полной) ларингэктомии удаляется вся гортань, подъязычная кость и несколько колец трахеи (в зависимости от распространения опухоли в подскладочный отдел). При выполнении полной ларингэктомии дыхательный тракт и пищеварительный тракт полностью отделяются друг от друга. Эффективность данной операции проверена временем, с ее помощью можно добиваться превосходных онкологических результатов. При наличии у пациента жалоб на затруднение дыхания, операция обычно начинается с трахеотомии, которая выполняется под местной анестезией. Чаще всего рекомендуется выполнение «верхней» трахеотомии, т.к. часть трахеи удаляется вместе с гортанью. При локализации первичного очага в надсвязочном отделе, либо при диагностированных метастазах в лимфоузлы, сначала выполняется двусторонняя шейная лимфодиссекция. При N0 достаточно выполнения двусторонней селективной лимфодиссекции. Затем разделяют надподъязычные и подподъязычные мышцы, верхний констриктор разделяется на уровне латеральной пластинки щитовидного хряща. Свободным элеватором вверху отслаивается слизистая оболочка грушевидных карманов, учитывая возможность использования для последующего сшивания глотки. Затем идентифицируют верхние и нижние паращитовидные железы и отводят их вбок на стороне первичного поражения, чтобы сохранить нижнюю щитовидную артерию. Со стороны первичного поражения обычно включается и доля щитовидной железы. Противоположная доля железы отсепаровывается от трахеи электрокоагулятором, при этом необходимо сохранить питающую ножку верхнего полюса и нижнюю щитовидную артерию. После разделения надподъязычных мышц мобилизуется подъязычная кость, большие рога отделяются от окружающих мягких тканей. При мобилизации верхнего рога в латеральном направлении нужно сохранить поъязычный нерв. Если трахеотомия уже выполнена, трахея рассекается на уровне трахеостомы. На трахею накладываются две 2-0 полипропиленовые лигатуры, чтобы предотвратить ее смещение в средостение. Задняя стенка трахеи отсепаровывается либо скальпелем № 15, либо коагулятором Bovie для создания «простенка» между пищеводом и трахеей. Место входа в глотку зависит от результатов предоперационной фиброскопии или непрямой ларингоскопии. Как правило, хирургу следует вскрыть глотку в месте, не затронутом опухолевым ростом, т.к. это позволит выделять гортань под контролем зрения. Этим местом могут быть валлекулы, грушевидные синусы или слизистая позадиперстневидной области. Наиболее быстрым вариантом является доступ через валлекулы. Определить нужное место рассечения глотки можно пропальпировав валлекулы пациента через ротоглотку аспиратором или небольшим крючком. После рассечения слизистой оболочки глотки, надгортанник берется на зажим. Хирург, стоя у изголовья пациента, изогнутыми ножницами рассекает глоточно-надгортанную складку, осторожно оставляя вокруг опухоли участок здоровых тканей. Разрез продолжается книзу. Размер сохраненной слизистой оболочки грушевидных синусов зависит от степени распространенности опухоли. Затем, после рассечения слизистой оболочки позадиперстневидной области, гортань может быть удалена. Если статус границ резекции неясен, следует отправить ткань с краев резекции на экспресс-исследование (также отправляются границы резекции на уровне трахеи). Для сохранения просвета трахеостомы в послеоперационном периоде выполняется пластика стомы (особенно важно, если в дальнейшем пациенту планируется проводить лучевую терапию). Одним из возможных вариантов является модифицированная W-пластика. Трахея рассекается вдоль двух колец по средней линии. Кожа вокруг стомы рассекается в форме буквы W. 2-0 полипропиленовыми нитями трахея подшивается к коже полупогружными матрацными швами. Затем, при помощи 2-0 полипропиленовых швов и 2-0 полиглактин 910 формируется нижняя часть стомы. Перед ушиванием глотки рассекается перстнеглоточная мышца. Если в дальнейшем планируется выполнение трахео-эзофагеальной пункции, на заднюю стенку трахеи ниже 1 см будущей стомы накладывается зажим. Затем в пищевод устанавливается резиновый катетер размером 14F. В некоторых центрах для питания в раннем послеоперационном периоде устанавливают назогастральный зонд, но при грамотном уходе питание может осуществляться и через катетер, который легче переносится больными, чем назогастральный зонд.
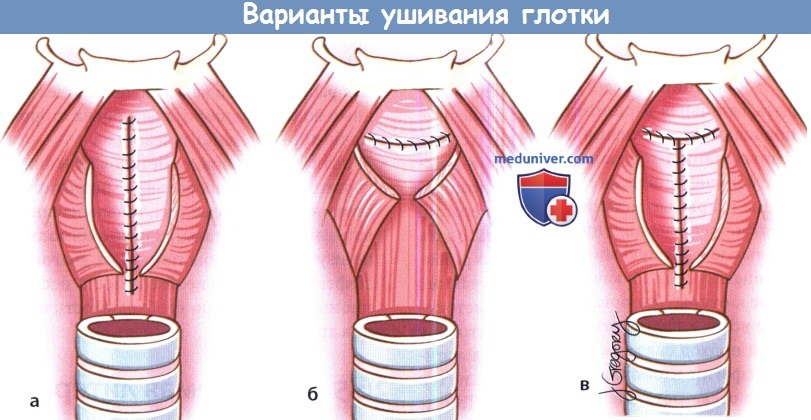
Методика ушивания глотки зависит от разных факторов (количество слизистой оболочки, предоперационная лучевая терапия, предпочтения хирурга). При наличии достаточного объема слизистой возможно вертикальное ушивание глотки обратным швом по Connel. Первый шов накладывается на уровне корня языка, затем слизистая глотки ушивается книзу по вертикали. По мере продвижения хирурга книзу опытный ассистент должен выворачивать края слизистой грушевидных синусов. Горизонтальное наложение швов обычно представляет большую сложность, особенно ближе к центру, поскольку здесь натяжение тканей максимально, особенно в центре Недостатком Т-образного ушивания глотки является образование трифуркации в центре (самое слабое место шва, где натяжение максимально). Но при правильном исполнении все три данных метода дают хорошие результаты. Для дополнительного укрепления глоточного шва возможно сшивание над ним волокон нижнего констриктора глотки вворачивающим швом, но данный метод увеличивает вероятность развития послеоперационной дисфагии. Для исключения просачивания слюны при помощи шприца в глотку вводится метиленовый синий. Места, в которых появился краситель, дополнительно ушиваются вворачивающим швом. Вне зависимости от метода ушивания глотки необходим тщательный послеоперационный уход для минимизации риска развития свища. Фибриновый клей, нанесенный на шов, также может снизить риск формирования фарингостомы. Если пациенту перед операцией проводилась лучевая терапия, реконструкция может выполняться по той же схеме, что была описана выше. Даже при достаточном объеме слизистой оболочки грушевидных синусов можно использовать другие методы реконструкции: пектораль-ный мышечно-кожный лоскут, свободный лучевой лоскут предплечья, свободный антеролатеральный лоскут бедра. Преимуществом этих методик является снижение риска формирования стриктур пищевода и глоточно-кожных фистул. Несколько групп исследователей описали успешное использование мышечного пекторального лоскута для профилактики формирования фарингостом у пациентов, которым выполняется «ларингэктомия отчаяния». Существуют различные методики восстановления голоса после ларингэктомии. У отобранных пациентов тра-хео-пищеводная пункция позволяет добиться появления понятной пищеводной речи. Кандидаты на выполнение трахеопищеводной пункции должны иметь хорошее (или корректируемое) зрение, хорошую координацию движений, а также быть надежными в плане послеоперационного наблюдения, т.к. клапаны требуется регулярно менять и чистить. Также существуют системы с режимом «свободные руки при разговоре», позволяющие говорить без закрытия клапана пальцем. Другим вариантом является использование аппарата «электрогортань», которая продуцирует «механический» голос при установке аппарата на шею или в полость рта (для последнего требуется специальный адаптер). Традиционно пациентам с рецидивом или сохранением заболевания после курса химиотерапии выполнялась тотальная ларингэктомия. Но в последние годы появляются сообщения о том, что у тщательно отобранных пациентов данной группы можно использовать эндоскопические лазерные или органосохраняющие открытые методики. В качестве операции отчаяния Steiner и соавт. предлагают использовать трансоральную лазерную микрохирургическую резекцию. Holsinger и соавт. в качестве операции отчаяния прибегают к открытым органосохраняющим методикам, чаще всего к надперстневидной ларингэктомии; но данный подход связан с увеличением риска аспирации, дисфагии и обструкции дыхательных путей вследствие отека оставшейся части гортани. Тем не менее, специалист по хирургии головы и шеи всегда должен помнить о существовании данных подходов в лечении рецидивирующих опухолей гортани.
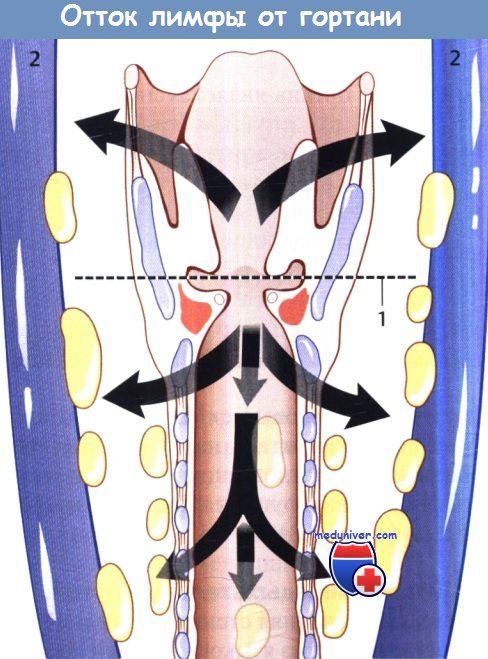
Лимфодиссекция при раке гортани. Решение о выборе метода воздействия на лимфоузлы шеи зависит от стадии первичной опухоли по системе TNM, пораженного отдела гортани, метода воздействия на первичную опухоль. На ранних стадиях рака голосового отдела относительно редко развиваются метастазы в регионарные лимфоузлы, поскольку лимфотток от этой области достаточно беден. У пациентов с раком голосового отдела гортани ранней стадии и статусом лимфоузлов N0 разумной стратегией является простое динамическое наблюдение. Надсвязочный отдел, напротив, характеризуется богатым двусторонним лимфоттоком в узлы яремно-двубрюшной цепи. И хотя в отдельных случаях опухоли Т1 можно прибегнуть к консервативной тактике, большинству пациентов с более распространенными опухолями необходимо селективное воздействие на лимфоузлы шеи (или хирургическое уровней II, III и IV, или лучевое, включающее зоны риска), вне зависимости от данных клинического осмотра. Если в лечении первичного очага использовалась лучевая терапия, центральные и латеральные лимфоузлы шеи также следует включать в поле облучения. При статусе лимфоузлов N+ выполняется соответствующая шейная лимфодиссекция. Ключевые моменты:
– Также рекомендуем “Показания и методика трансоральной роботизированной хирургии (TORS)” Оглавление темы “Болезни слюнных желез и гортани”:
|
Источник