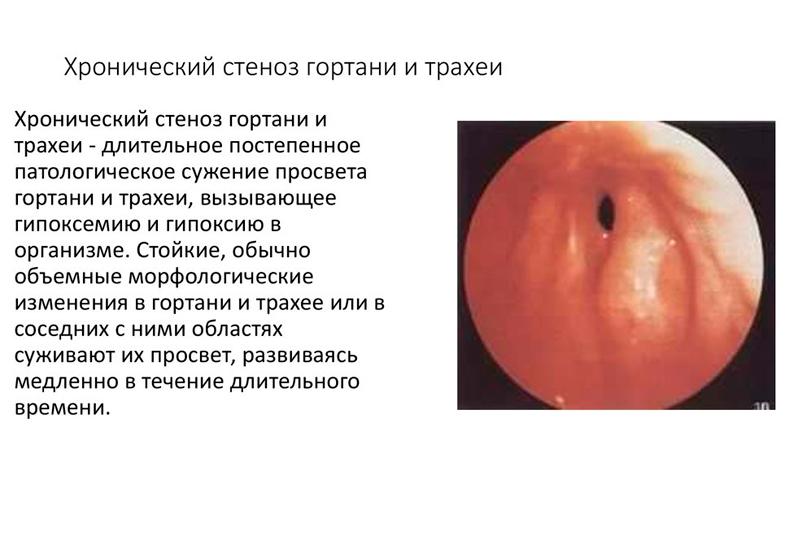
Хронический паралитический стеноз гортани

Хронический стеноз гортани — это постепенно возникающее полное или частичное сужение просвета гортани. Оно сопровождается снижением проступания в дыхательные пути количества воздуха и в результате может привести к кислородному голоданию вашего организма, а иногда даже и к асфиксии.
Содержание статьи:
- Причины появления хронического стеноза гортани
- Симптомы хронического стеноза гортани
- Диагностика заболевания хронический стеноз гортани
- Осложнения хронического стеноза гортани
- Принципы лечения хронического стеноза гортани
Причины появления хронического стеноза гортани
Постоянными причинами, которые могут спровоцировать появление хронического стеноза гортани будут: аномалии развития, травмы гортани, опухоль гортани, инфекционные и травматические артриты, воспаление надхрящницы и самого хряща, а также и их осложнения, нейропатический парез гортани, попадание в горло инородных предметов, различные аллергические реакции, хирургические рубцы, двусторонний шейный лимфаденит, злокачественные опухоли и доброкачественные образования, черепно-мозговые травмы, ожоги гортани, нарушение деятельности нижнегортанных нервов, а также воспалительные заболевания.
Иногда возникает хронический стеноз как следствие неправильно выполненной трахеотомии (введения через разрез первого кольца трахеи трахеотомической трубки в гортань), неправильный подбор трубки или ее длительное и неправильное ношение.
Симптомы хронического стеноза гортани
Основные симптомы болезни хронического стеноза гортани в первую очередь напрямую зависят от самой стадии заболевания и степени сужения гортанной щели, присутствия опухолей. Отоларингология на сегодняшний день выделяет 4 стадии в хроническом стенозе гортани: компенсированную стадию, субкомпенсированную стадию, декомпенсированную стадию и стадию удушья.
Первая стадия болезни характеризуется более редким и углубленным дыханием, выпадением пауз между вдохом и выдохом, значительным уменьшением числа вдохов, а также заметным нарушением соотношения между нормальным пульсом и сопутствующими дыхательными движениями. На второй субкомпенсированной стадии, исходя из степени сужения гортанной щели и от того, как долго протекает болезнь, организм больного сам постепенно начинает дышать через суженый просвет. При тяжелых физических нагрузках дыхание затрудняется, а в состоянии спокойствия выравнивается.
На этой стадии реакции приспособления могут быть дыхательными, гемодинамическими, кровяными, тканьевыми. При дыхательном привыкании учащается дыхание, присутствует постоянная одтышка, а также в дыхании участвуют нехарактерные для этого процесса мышцы. Повышенное давление и ускорение тока крови становится постоянным, повышается проницаемость сосудов, а также появляется большое количество эритроцитов в крови, таким способом организм человека пытается насытить кровь необходим количеством кислорода. Но такие приспособительные механизмы срабатывают до определенного момента. С течением времени гипоксия все-таки увеличивается и приводит к появлению третьей степени хронического стеноза гортани.
В течение третий стадии декомпенсации в организме человека уже отчетливо проявляются все ключевые признаки начальной асфиксии и гипоксии. Возникает посинение слизистых оболочек, кожных покровов непосредственно вокруг ротовой полости, под глазами и белков глаз, происходит втяжение межреберных промежутков, при вдохе резкое втяжение яремной ямки и подключичных ямок, дыхание человека становится очень частым и сопровождается неким шумом при вдохе воздуха, также у больного появляется холодная испарина, голос пропадает и человек не говорит или может только шептать. Четвертая стадия — это стадия полной асфиксии или удушья, при ней ухудшается сердечная деятельность человека, дыхание больного становится поверхностным и достаточно редким, зрачки расширяются, кожа синеет, тело становится безучастным к внешним раздражителям, вялым. Возможно неконтролируемое отхождение кала и мочи, постоянная потеря сознания и в конечном итоге остановка дыхания.
При длительном стенозе хронического типа в организме больного тоже могут включаться приспособительные функции, которые направленны на стабильное обеспечение организма человека необходимым объёмом кислорода. При этом как на второй стадии развития болезни наблюдается учащение пульса, ускорение кровотока, гипотония, отдышка, учащенное дыхание с участием мышц спины, шеи и плеч. Также сделав определенные анализ крови можно заметить, что во всех живых клетках запускаются анаэробные процессы, а также появляется гипертрофия мышцы сердца. При хроническом стенозе гортани, в связи с постоянной потребностью ношения трахеотомической трубки, временно отключаются функции увлажнения, согревания верхних дыхательных путей, а также механической и биологической очистки воздуха.
Диагностика заболевания хронический стеноз гортани
Главным намерением в проведении диагностики является не так постановка диагноза, как определение главной причины возникновения хронического стеноза гортани. Диагностика заболевания в большинстве случаев основана на жалобах пациента, симптомах, анамнезе и на результатах таких исследований как:
- ларингоскопия, биопсия;
- бронхоскопия;
- рентгенологическое исследование;
- эндоскопическое исследование.
При определении диагноза может потребоваться КТ гортани, ультразвуковое исследование щитовидной железы, МРТ головного мозга, также бактериологическое исследование мазков из открытого зева и рентгенография пищевода больного.
Осложнения хронического стеноза гортани
Острая нехватка внешнего дыхания при хроническом стенозе гортани приводит к застойным скоплениям мокроты в дыхательном пути, что является частой причиной пневмоний и бронхита. У больных с трахеостомой воздух, поступающий в трахею, не согревается, не увлажняется и не очищается, что в нормальном здоровом организме происходит в верхних дыхательных путях. В таких случаях очень часто развиваются трахеиты и трахеобронхиты, а бронхиты имеют хроническое течение. Заболевания легких в виде затяжной пневмонии, приводят к бронхоэктатической болезни. Большая нагрузка на правый отдел сердца и малый круг кровообращения ведет к появлению легочной гипертензии и развитию у пациента легочного сердца.
Принципы лечения хронического стеноза гортани
При появлении симптомов удушья, следует немедленно вызвать скорую помощь. Еще до приезда врачей, нужно успокоить больного, растереть ему руки и ноги, в помещении увлажнить воздух или же поместить больного в ванную, набрав в нее предварительно горячую воду. Будьте готовы к тому, что больного госпитализируют. Не пугайтесь, но первые несколько дней лечение будет происходить в отделе реанимации.
Выбор метода лечения напрямую зависит от первостепенного заболевания, которое спровоцировало хронический стеноз гортани и от стадии самого стеноза. Лечение может быть медикаментозным и хирургическим. Если причиной болезни стало предварительное инфекционное заболевание, в первую очередь применяется антибактериальная терапия с использованием антигистаминных препаратов, которые снимут аллергический отек. У детей причиной часто может быть посторонний предмет, но его самостоятельное извлечение в условиях за пределом клиники запрещено.
Хирургическое вмешательство может в себя включать введение трубки, что будет препятствовать сужению гортани, дилатацию Т-образными трубками, рассечение передней стенки гортани, растягивание гортани дилятаторами и бужами.
В хирургических случаях лечения хронического стеноза гортани, больному обязательно нужна операция, которая будет происходить следующим образом: в полусидячем или лежачем положении больному вводят анестезию, в случаях полной асфиксии операция проводится безо всякой анестезии, чтобы не упускать ни единой минуты. Обезболивание местного характера — 1% новокаина с примесью адреналинового раствора 1:1000 (1 капля на 5 миллилитров). После анестезии начинают прощупывать подъязычную кость у пациента, вырезку щитовидного хряща и бугорок перстневидного хряща. Для того чтобы лучше ориентироваться, бриллиантовой зеленью отмечают срединную линию, а также уровень перстневидного хряща. Далее делают послойный разрез кожи больного и подкожной клетчатки на 6 сантиметров вертикально книзу строго по намеченной серединной линии, начиная от нижнего края перстневидного хряща. Разрезают поверхностную фасцию, под ней обнаруживается место, где соединяются грудино-подъязычные мышцы. Подъязычную мышцу надсекают и тупым путем раздвигают мышцы. Просматривается перешеек щитовидной железы, на ощупь он очень мягкий и характеризуется коричнево-красным цветом. По нижнему краю перстневидного хряща разрезают капсулы железы, что фиксирует перешеек. Перстневидный хрящ смещается книзу и его удерживают крючком с тупым концом. После этого будет видно кольца самой трахеи, покрытые фасцией. Необходим тщательный гомеостаз до вскрытия трахеи. Для фиксации гортани вкалывают крючок с острым концом в щитоподъязычную мембрану и фиксируют. Для того чтобы избежать кашля, через иглу вводят пару капель 2-3% раствора Дикаина в трахею, затем вскрывают 2 и 3 кольца трахеи остроконечным скальпелем. Сам скальпель нужно вонзить не глубоко, примерно 0,5 сантиметров, чтобы случайно не поранить заднюю стенку трахеи, что лишена хряща и прилегающую переднюю стенку пищевода. С помощью расширителя Труссо края в трахее аккуратно раздвигают и вводят трахеотомическую трубку соответствующего размера, ее фиксируют на шее больного марлевой повязкой. В детской лечебной практике при хроническом стенозе гортани, который вызван дифтерией трахеи и гортани, используется назо(оро)трахеальный вид интубации с помощью гибкой трубки, сделанной из качественного синтетического материала. Интубация проводится строго под прямой ларингоскопией. Если необходим длительный срок интубации, будет производиться трахеотомия, потому что более длительное пребывание трубки в гортани, может вызвать ишемию слизистой оболочки с дальнейшим рубцеванием и стойким стенозом дыхательного органа.
Все это достаточно сложные операции, которые могут включать много этапов, но в большинстве случаев они дают очень хороший результат.
Послеоперационная терапия включает в себя: профилактику осложнений гнойно-воспалительного характера, улучшение микроциркуляции в послеоперационной области, профилактику вторичного рубцевания, уменьшение общей и локальной гипоксии, повышение реактивности организма и лечение сопутствующих болезней, коррекцию гормональных отклонений и сердечно-сосудистых нарушений у больного.
Эффективность лечения пациентов со стенозом гортани различной этиологии, докторами оценивается по таким параметрам:
- восстановление нормального просвета в дыхательном пути;
- факт декануляции;
- возвращение к больному стабильной дыхательной функции, голосовой способности и разделительной функции;
- учитывается продолжительность лечения и хирургических вмешательств;
- наблюдается динамика показателей газового и кислотно-щелочного состава крови, сердечной деятельности и дыхательной функции.
На сегодняшний день, хронический стеноз гортани полностью излечимо, главным фактором является стадия, на которой оно обнаруживается у пациента. При обнаружении хотя бы одного из выше наведенных симптомов, обязательно обратитесь к врачу и болезнь можно будет предотвратить на медикаментозном уровне без госпитализации.
Источник
В статье представлен алгоритм выбора тактики хирургического лечения больных со стенозами гортани
Проблема диагностики и лечения хронических паралитических и сочетанных стенозов гортани находится под пристальным вниманием оториноларингологов, хирургов, реаниматологов. В 75–95% случаев причинами стенозирования гортани и трахеи являются возросшая хирургическая активность на органах шеи с поражением ветвей блуждающего нерва, различного рода травмы гортани и нередко последствия хирургического лечения ее паралитических стенозов. Рубцово-паралитический стеноз гортани занимает 2-е место по частоте (29,9%) в структуре хронических заболеваний голосового аппарата [1–3].
Существующие методы диагностики и хирургического лечения больных многоэтапны, требуют значительных затрат на лечение, не всегда эффективны. Использование новых технологий и опорных материалов в реконструктивной хирургии позволяет реабилитировать большинство пациентов со стенозом гортани и трахеи травматической этиологии. Диагностика данной патологии стала возможной с появлением видеофиброларингоскопии, видеостробоскопии, магнитно-резонансной томографии (МРТ), спиральной компьютерной томографии. Тщательное дооперационное обследование позволяет выбрать оптимально эффективный способ первичного оперативного вмешательства, т. к. при его неудачном результате исчерпывается запас здоровой ткани, и паралитический стеноз гортани переходит в рубцово-паралитический [1, 5].
Реконструктивная хирургия гортани и трахеи на современном этапе развивается в 2-х основных направлениях: совершенствование хирургической техники и разработка мер профилактики послеоперационных осложнений; профилактика рестенозирования сформированного просвета в раннем и позднем послеоперационном периоде. Ларинготрахеопластика в сочетании с протезированием гортани и трахеи является наиболее перспективным методом, позволяющим восстанавливать анатомическую целостность органа и его функции [1, 3, 5, 8]. В настоящее время используются экстраларингеальные, эндоларингеальные (с наружным и эндоскопическим доступом) методы реконструктивной хирургии. Общепринятыми способами лечения травматических стенозов гортани являются эндоларингеальные хирургические вмешательства с наружным доступом с последующим разведением и фиксацией фрагментов гортани [9–11].
Рациональное стентирование на заключительном этапе операции необходимо для сохранения созданного просвета гортани. Формирование гортанно-трахеального просвета на Т-образной трубке является наиболее физиологичным, т. к. позволяет больным на время лечения сохранить гортанное и носовое дыхание. Нередко в раннем послеоперационном периоде нарушается защитная функция гортани из-за давления краниального конца трубки на основание надгортанника и черпало-надгортанные складки: слюна и пища попадают в дыхательные пути [8, 11, 12]. Важным является индивидуальный подбор эндопротеза с учетом строения шеи и конституции тела. Разработаны схемы ведения больных в послеоперационном периоде, включающие антибактериальную, антиоксидантную терапию, нестероидные противовоспалительные и улучшающие репарацию тканей препараты, физиотерапию и сеансы гипербарической оксигенации [1, 8].
C целью повышения эффективности хирургического лечения больных посттравматическими стенозами гортани разработан алгоритм выбора оперативной тактики, основанный на учете индивидуальных особенностей стереоморфометрических характеристик структур гортани у людей различного пола, с различным телосложением и строением шеи. Алгоритм включает: антропометрию пациента – определение варианта строения шеи и телосложения; построение регрессионных моделей значимых ларингометрических параметров; выбор оптимальной технологии ларингопластики в зависимости от клинических данных – размеров голосовой щели и положения голосовых складок; расчет размеров аутотрансплантата и длины Т-образной трубки, основанный на математическом анализе антропо- и органометрических характеристик пациента; ларинготрахеопластику и протезирование сформированного гортанно-трахеального просвета для предупреждения рецидива стеноза и рубцевания в отдаленном послеоперационном периоде.
Материал и методы
Под наблюдением с 2004 по 2015 г. находился 71 пациент в возрасте от 23 до 68 лет с хроническим посттравматическим стенозом гортани. Первичных больных было 65, остальные 6 были ранее оперированы: количество предыдущих операций составило от 1 до 5, а сроки лечения – от нескольких месяцев до 7 лет. Проводилось оториноларингологическое и общеклиническое обследование всех больных: тщательный сбор анамнеза, определение степени тяжести сопутствующей патологии. Использованы также антропометрия и объективные методы, характеризующие степень протяженности и характер патологического процесса (эндофибробронхоскопия, стробоскопия, спирометрия, рентгенотомография, компьютерная томография (КТ) гортани и трахеи).
Осуществлялся сравнительный анализ историй болезни пациентов с данной патологией, оперированных в клинике в периоды с 1996 по 2003 г. (n=24) и с 2004 по 2015 г. (n=71). У 24 больных (клиническая группа I – архивная) с паралитическими и сочетанными стенозами гортани изучались результаты хирургического лечения экстраларингеальным методом без учета конституции пациента и анализировались показатели деканюляции в отдаленном послеоперационном периоде (1 год). В клиническую группу II был включен 71 пациент с хроническим стенозом гортани, обследованный на дооперационном этапе с помощью антропометрии, спирометрии, КТ и фиброларингоскопии, оперированный по усовершенствованным методикам с учетом варианта строения шеи и телосложения. Первым этапом выполнялась трахеостомия, вторым – отсроченная (через 1–1,5 мес.) ларинготрахеопластика. Оценка эффективности лечения больных II группы (n=71) проводилась по критериям: деканюляция, динамика показателей функции внешнего дыхания (ФВД) и интенсивность голоса до и после ларингопластики (в отдаленном послеоперационном периоде).
Пациенты клинической группы II (n=71) оперированы с использованием следующих усовершенствованных методик с учетом варианта строения шеи и телосложения:
– экстраларингеальная ЛФ ГС (n=22);
– ЛФ ГС со стентированием Т-образной силиконовой трубкой (n=43);
– рассечение рубцов после предыдущих ларингопластик с последующим стентированием гортани (n=6).
Согласно разработанной и примененной в клинике методике конституциональной ларингостереотопометрии [патент № 48738 РФ] у больных дооперационно по антропометрическим данным и регрессионным моделям (p<0,05) определялись необходимые при проведении ларингопластики параметры гортани, а также размеры Т-образного эндопротеза и хрящевого аутотрансплантата под переднюю треть голосовой складки [4, 6, 7].
22 пациентам (31%) с хроническим паралитическим стенозом производилась ЛФ ГС с аритеноидотомией [патент № 2284773 РФ], включающая экстраларингеальный подход к пластине щитовидного хряща спереди, поднадхрящничную резекцию голосового отростка черпаловидного хряща с иссечением внутренней перстнещитовидной и большей части щиточерпаловидной мышц; укладывание аутохряща под переднюю треть голосовой складки; отведение эластического конуса с голосовой складкой путем наложения лигатур и затягивание их на аутотрансплантате, наложенном на пластину щитовидного хряща. Резекция голосового отростка черпаловидного хряща с иссечением щиточерпаловидной и внутренней перстнещитовидной мышц приводит к расширению межскладкового пространства и улучшению дыхательной функции, а подведение предварительно смоделированного по регрессионным моделям аутохряща перегородки носа под переднюю треть голосовой складки способствует сохранению голосовой функции [4, 6].
Пациентам с имеющимся рубцовым процессом в голосовом отделе (60,6%) от предыдущих вмешательств (n=43) после выполнения экстраларингеальной ЛФ ГС (рубцово-неизмененной) с аритеноидотомией выполнялось стентирование гортани и трахеи силиконовой Т-образной трубкой с предварительной коррекцией ее краниального и каудального отрезков [7]. У 6 пациентов с подголосовым стенозом (8,45%) после многократных вмешательств на голосовых складках рубцовая ткань после рассечения распределялась по периметру гортани и трахеи для уменьшения сроков эпителизации сформированного просвета на Т-образном эндопротезе. Во избежание рестенозирования в подскладковом пространстве проводились редрессация перстневидного хряща и формирование боковых стенок трахеи с помощью кожно-васкуляризированных лоскутов.
Таким образом, у 49 пациентов (69%) после ларингопластики проводилось стентирование сформированного ларинготрахеального просвета силиконовой Т-образной трубкой, предварительно смоделированной с учетом антропометрических данных и регрессионных моделей [патент № 2432969 РФ]. Существует 2 вида наиболее применяемых Т-образных силиконовых трубок у взрослых (ЗАО «Медсил»): «ТЭТсО-13/23-45/70/40» (длина краниального отрезка – 45 мм, каудального отрезка – 70 мм, диаметр овального отводящего конца – 13/23, длина – 40 мм) и «ТЭТсК-15/15-50/80/60» (длина краниального отрезка – 50 мм, каудального отрезка – 80 мм, диаметр круглого отводящего конца – 15/15, длина – 60 мм). Заводская длина краниального отрезка 45–50 мм практически всегда превышает необходимую после ларингопластики, особенно у пациентов с толстой и короткой шеей. Разработанная и примененная в клинике методика коррекции длины Т-образной трубки основана на математическом анализе органо- и антропометрических характеристик пациента: длины и окружности шеи, длины тела, акромиального диаметра, окружности грудной клетки. Составлены регрессионные уравнения для расчета длин отрезков Т-образной трубки по антропометрическим данным для мужчин и женщин (p<0,05) [7]. Смоделированная трубка «ТЭТсО–13/23-45/70/40» вводилась на созданное анатомо-функциональное ложе после ларингопластики. У 4-х пациентов (5,8%) наблюдалось нарушение защитной функции гортани в раннем послеоперационном периоде, которое разрешилось после коррекции длины краниального отрезка эндопротеза под контролем фиброларингоскопии. При смене эндопротеза в раннем послеоперационном периоде во избежание травм слизистой гортани и кожно-трахеальных швов проводились тракции на себя и книзу, при этом краниальный конец стента придерживался изогнутым зажимом в просвете трахеи до момента его складывания, после чего трубка извлекалась. Перед введением трубки ее наружную поверхность покрывали слоем лечебной мази. Сначала устанавливался каудальный отрезок для предотвращения гипоксии, затем – краниальный. Расположение последнего выше голосовых складок и зоны реконструкции контролировалось методом непрямой ларингоскопии и фиброларингоскопии, после чего наружное колено трубки закрывалось герметично притертой пробкой, при этом дыхание через естественные пути не должно быть затрудненным.
Этиотропная и патогенетическая терапия в послеоперационном периоде проводилась с учетом микробного пейзажа раневого отделяемого и чувствительности выделенных микроорганизмов к антибиотикам. Использовались препараты местного действия: мази с антибактериальным и противовоспалительным действием (в состав которых входят хлорамфеникол и мупироцин), а также содержащие гепариноиды и ангиопротекторы. В течение первых 5 сут после операции проводилась регулярная санация трахеобронхиального дерева с помощью эндофибробронхоскопии и катетеризации через Т-образный стент. Ингаляции муколитиков, антибиотиков и стероидных препаратов проводились 2 р./сут через естественные дыхательные пути с закрытым Т-образным стентом и трахеостому в первые 3–5 сут. Все пациенты были выписаны на 17–21-е сут после операции, обучившись самостоятельной смене и туалету Т-образной трубки. Динамическое наблюдение за больными после выписки из стационара должно проводиться каждые 10 дней. При контрольном осмотре методом фиброларинготрахеоскопии оценивались адекватность протезирования, размер гортанно-трахеального просвета и состояние слизистой оболочки гортани и трахеи на уровне верхнего и нижнего сегментов Т-образной трубки. Рецидивов стеноза не последовало, что подтверждено исследованиями ФВД в ближайшем и отдаленном (1 год) послеоперационном периоде. На заключительном этапе реабилитации через 6–8 мес. проводилось ушивание ларинготрахеального дефекта по Бокштейну после контрольного периода наблюдения в стационаре с герметично заклеенной ларинготрахеостомой.
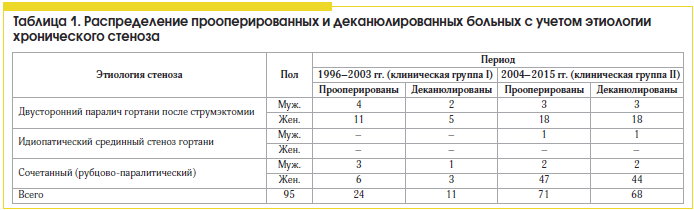
Проанализированы результаты хирургического лечения больных с хроническими стенозами гортани (n=71), у которых в предоперационном планировании ларингопластику и подбор оптимальных размеров эндопротеза и аутотрансплантата осуществляли с учетом регрессионных моделей (2004–2015 гг.). Они были сопоставлены с результатами хирургического лечения больных (n=24), проведенного традиционным методом без использования регрессионных моделей и антропометрических данных пациента (1996–2003 гг.). Учитывали наличие технических интра- и послеоперационных осложнений; неадекватные размеры эндопротеза и трансплантата; наличие грануляций и хондроперихондрита хрящевых структур; прорезывание латерофиксирующего шва и дислокацию голосовой складки к средней линии; нарушение защитной функции гортани в послеоперационном периоде (табл. 1). В клинической группе I (архивной) из 24 пациентов, оперированных экстраларингеальным доступом без учета шейного индекса и конституции, было деканюлировано 11 больных (45,8%). У 6 пациентов в раннем послеоперационном периоде латерофиксирующие швы прорезались в связи с присоединившимся отеком и гематомой подскладкового пространства; у 5 больных наблюдался хондроперихондрит гортани.
В клинической группе II (n=71) оценка динамики показателей ФВД и интенсивности голоса до и после ларингопластики (1 год) проводилась раздельно у пациентов с паралитическими (n=22) и сочетанными (n=49) стенозами гортани.
После хирургического лечения у 22 (31%) пациентов с паралитическим стенозом гортани методом экстраларингеальной ЛФ ГС с аритеноидотомией основные показатели ФВД приблизились к условной норме, а индекс Тиффно – к норме, что клинически соответствует компенсации стеноза гортани. Подведение под переднюю треть голосовой складки смоделированного по регрессионным моделям аутотрансплантата позволило сохранить и незначительно улучшить интенсивность голоса – с 57,4±0,2 до 59,7±0,2 дБ.
Хирургическое лечение и дилатация сформированного просвета Т-образной силиконовой трубкой проводились у 49 (69%) пациентов клинической группы II. В данной подгруппе больных с хроническим сочетанным стенозом гортани применен способ подбора длины Т-образной трубки [7], основанный на математическом анализе антропо- и органометрических характеристик пациента. Через 8 мес. основные показатели ФВД приблизились к нормальным значениям и выросли на 14,5–29,3%, а индекс Тиффно – на 33,6%.
Сравнительный анализ эффективности хирургического лечения 95 больных с посттравматическими стенозами гортани за периоды с 1996 по 2003 г. (n=24, клиническая группа I) и с 2004 по 2015 г. (n=71, клиническая группа II), когда дооперационно стало проводиться прогнозирование ларингометрических параметров по шейному индексу пациента и антропометрическим данным, показал, что количество деканюлированных пациентов увеличилось с 45,8 до 95,8% (см. табл. 1). Из 71 пациента с посттравматическими стенозами гортани дыхательная функция была восстановлена у 68 (95,8%).
С учетом разработанной и примененной методики конституциональной ларингостереотопометрии разработан алгоритм выбора тактики хирургического лечения больных с параличами и сочетанными стенозами гортани. По антропометрическим данным для каждого пациента клинической группы II (n=71) дооперационно были построены регрессионные модели необходимых ларингометрических параметров, выбрана оптимальная технология ларингопластики в зависимости от клинических данных – размеров голосовой щели и положения голосовых складок (рис. 1).

В результате использования предложенного алгоритма выбора тактики оперативного лечения полная реабилитация наступила у 68 (95,8%) больных с хроническим стенозом гортани. Таким образом, конституциональный подход к предоперационному планированию и хирургическому лечению больных с посттравматическими стенозами гортани позволяет прогнозировать восстановление анатомической архитектоники полых органов шеи и оптимальное течение послеоперационного периода, избегать осложнений, повышать процент надежной стабилизации просвета дыхательных путей и ранней реабилитации пациентов. В случае недостаточного учета изменчивости размеров гортани возникают явления хондроперихондрита гортани, в дальнейшем – избыточное рубцевание в зоне реконструкции, что увеличивает одновременно с кратностью вмешательств и сроки инвалидизации пациентов.
Источник