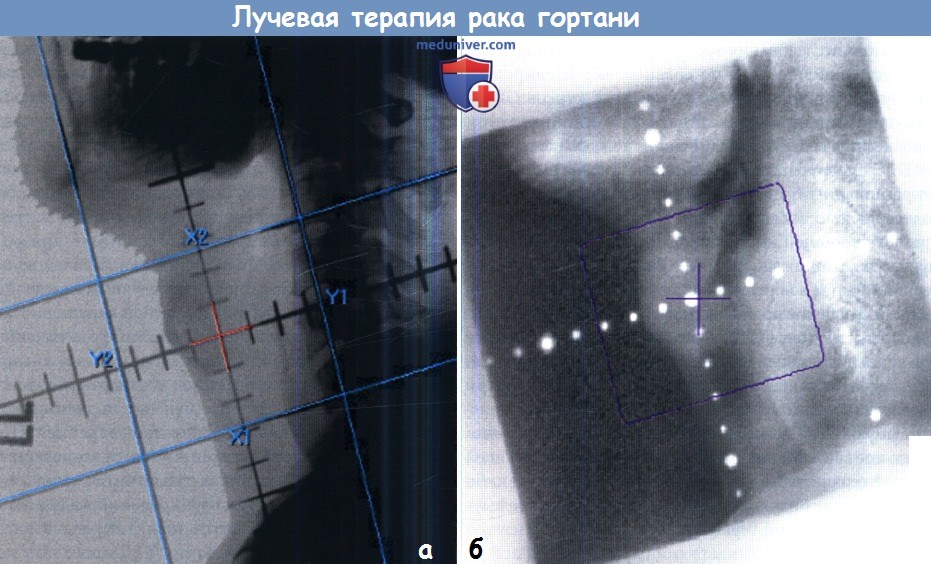
Химиолучевая терапия при раке гортани
анонимно, Женщина, 23 года
Добрый день! Моему папе 54 года. В январе 2015г он обнаружил уплотнение в горле, которое со временем росло и только в июне он обратился за мед. Помощью поставили страшный диагноз- рак ротоглотки, 4 степень. Провели химиолучевое лечение, вследствие которого намека на опухоль не осталось. Должна сказать, что лечение папа перенес хорошо, самостоятельно питался, полоскал постоянно горло антисептиками. После лечения была проведена операция ( метостазы в лимфоузле). Спусти месяц после операции начался сильный кашль (поставили фиброз послучевой), жуткие боли в шее-отдающие в голову, боль в горле до невозможности глотать слюну, сильный отёк шеи. Лежать он может только в одном положении. Поставили назогастральный зонд, т.К. Самостоятельно питаться уже было невозможным. Папа сильно похудел. Были моменты, когда из за сильного мокрого кашля он начинал задыхаться ( послучевой эпителиит). Врачи разводят руками, своё дело сделали-лечение провели, а вот как восстанавливаться никто не говорит. Порекомендовали провести противовоспалительную и противоотечную терапию, в случае необходимости сделать трахеостомию. Для снятия отека и хоть как то облегчить дыхания прописали дексаметазон ( но ведь мы не можем ставить его постоянно). Дайте совет, как папе помочь.И что включает в себя противоотечная и противовоспалительная терапия? Заранее спасибо!
Добрый вечер. К сожалению осложнения которые имеют место быть у вашего папы являются частыми у пациентов, перенесших такое лечение, хотя вы описываете довольно тяжелую степень лучевого повреждения. Что касается реабилитации, то действительно нужно продолжать противоотечную терапию можно попробовать ингалляции с гидрокортизоном и флуимуцилом – поможет снять отек и улучшит отхаркивание. Постановка трахеостомы в данном случае даже желательна, потому что его постоянный кашель может быть следствием хронической аспирации слюны на фоне постлучевого пареза гортани – достаточно частое осложнение, т.е. гортань не полностью прикрывает дыхательные пути во время глотания, а во время вдоха подсасывается мокрота, что в свою очередь вызывает бронхиты и бронхопневмонии. Если поставить трахеостому с манжетой, то это отграничит дыхательные пути.
Длительное ношение назогастрального зонда тоже вызывает хроническое воспаление в этой области, а также может вызвать ряд более грозных осложнений. Перкутанная эндоскопическая гастростомия – (трубочка на передней брюшной стенке) достаточно простой и относительно безопасный способ наладить питание у таких пациентов и избавить от необходимости ходить с зондом. Ну и конечно адекватное обезболивание. Процесс восстановления при таких случаях очень длительный, но вы можете помочь своему папе. Реабилитация таких пациентов это очень важная задача, которая увы, соглашусь с вами, часто остается без должного внимания. Доброго здоровья.
анонимно
Большое спасибо,за развернутый ответ. Сегодня установили трахеостому,дышать стало легче. Подскажите,пожалуйста,через какое время дышать можно будет естесственным путем?? Папа не сможет говорить в течении всего времени,пока у него стоит эта трубка?или речь врсстановится?сейчас он пишет на листочке..спасибо!!!
Источник
Методы консервативного лечения рака гортани – без операцииМеждисциплинарное обследование пациентов с раком гортани включает консультацию онколога-радиолога. Рак голосовой щели ранних стадий очень редко мета-стазирует в регионарные лимфоузлы, поэтому у таких пациентов можно использовать лишь один метод воздействия, которым с полным правом может быть лучевая терапия. Лучевая терапия имеет свои преимущества, к которым относятся неинвазивность, приемлемое сохранение голосовой функции, превосходный контроль местного опухолевого роста. У пациентов с заболеванием на ранней стадии обычно удается достичь превосходных функциональных результатов, а побочные эффекты носят временный характер (ксеростомия, мукозит, дисфагия, местные воспалительные реакции). Благодаря совершенствованию методов лучевой терапии, а именно изобретению лучевой терапии модулированной интенсивности (ЛТМИ), при низком риске регионарных метастазов возможно подвергать облучению лишь саму гортань, избегая поражения других органов головы и шеи. И хотя качество голоса после лучевой терапии почти всегда ухудшается, у большинства пациентов с раком ранних стадий голос возвращается до почти нормального уровня в течение года после завершения лучевой терапии. Использование лучевой терапии при опухолях Т1 стадии позволяет добиться подавления опухолевого роста в 90% случаев. Показатели при опухолях стадии > Т2 не столь впечатляющие, но тоже приемлемые (80%). Следует отметить, что, согласно опубликованным данным, в случаях поражения передней комиссуры первичное лечение при помощи лучевой терапии обычно менее эффективно. Использование лучевой терапии на ранних стадиях рака надскладочного отдела также позволяет добиться подавления опухолевого роста в 90% случаев. Поскольку надскладочный отдел имеет более богатую сеть лимфатических сосудов, доза облучения, получаемая пациентами, выше, чем при опухолях складочного отдела, т.к. воздействовать необходимо и на лимфоузлы шеи. Конкретные алгоритмы лечения в каждом учреждении разные, может использоваться как однократное каждодневное облучение, так и курсы гиперфракционирования или ускоренные схемы.
Запущенные формы рака гортани (III и IV) традиционно лечились хирургически с возможной послеоперационной лучевой терапией, однако положение дел изменила публикация фундаментального исследования рака гортани, выполненное в 1991 году исследовательской группой Американского министерства по делам ветеранов, согласно которому индукционная химиотерапия с последующей лучевой терапией позволяет добиться лучшего сохранения функций гортани, не снижая при этом показатели выживаемости. За последние 20 лет химиолучевая терапия в лечении распространенных форм рака гортани стала использоваться гораздо чаще. Изменение протокола внесло и свои недостатки, поскольку интенсивная химиолучевая терапия сопровождается развитием серьезных побочных эффектов, к которым относятся длительная дисфагия и ксеростомия. Использование больших доз облучения увеличивает риск развития тяжелых осложнений, например, остераднекроза гортани, который может потребовать трахеотомии и даже ларингэктомии даже при отсутствии рецидива опухолевого роста. Одновременно с описанным выше поворотом в подходах к лечению, Hoffman и соавт., проанализировав данные Национальной базы данных по онкологическим заболеваниям (National Cancer Data Base), отметили снижение выживаемости пациентов с раком гортани на протяжении 1985-2001 годов. Причины данного спада в выживаемости до конца не ясны. Согласно современным рекомендациям Американского сообщества клинических онкологов, у всех пациентов с раком гортани Т1-Т2 рекомендуется использовать органосохраняющие методы лечения (как хирургические, так и нехирургические). У пациентов с опухолями Т3 и Т4, не прорастающими через хрящи гортани в мягкие ткани, допустима органосохраняющая химиолучевая терапия. Могут использоваться либо неоадъювантная химиотерапия с последующей химиолучевой терапией, либо модифицированные схемы химиолучевой терапии. Выбор химиопрепаратов достаточно широк, от традиционных препаратов платины (цисплатин), до моноклональных антител и антагонистов рецепторов эпителиального фактора роста (цетуксимаб). При выборе между послеоперационной лучевой или химиолучевой терапией необходимо учитывать несколько факторов. Во-первых, определяется распространение процесса (положительные или неясные края резекции опухоли, инвазия в кровеносную или лимфатическую систему, внеларингеальный рост). Также необходимо оценить наличие метастазов в лимфоузлы шеи. Назначение адъювантного лечения проводится совместно с онкологами.
Ключевые моменты: – Вернуться в оглавление раздела “отоларингология” Оглавление темы “Болезни глотки и гортани”:
|
Источник
Методы лучевой терапии при раке гортаноглотки
Пациенты с заболеваниями на ранних стадиях составляют около 25% всех случаев рака гортаноглотки. У пациентов с операбельными опухолями Т1-Т2 необходимо добиться и местно-регионарного контроля опухолевого роста, и сохранения функций глотания и голосообразования.
Достичь этого можно либо использованием консервативных оперативных вмешательств, либо лучевой терапией. Выполнение шейной диссекции показано даже пациентам с N0, поскольку у 30-40% из них имеется риск развития скрытых метастазов.
На ранних стадиях плоскоклеточного рака гортаноглотки (T1 или опухоль Т2 малых размеров, не распространяющаяся до уровня перстневидного хряща) может применяться наружная дистанционная лучевая терапия. При использовании лучевой терапии уничтожаются ранние и скрытые метастазы лимфоузлов, поэтому пропадает необходимость в выполнении шейной лимфодиссекции. Успешность местно-регионарного контроля опухолевого роста в стадиях Т1-Т2 при помощи лучевой терапии сильно варьирует в разных исследованиях, также она зависит от техники и дозы облучения, критериев отбора пациентов, вовлечения лимфоузлов.
В целом, уровень местно-регионарного контроля варьирует от 47% до 90%, а пятилетняя выживаемость от 11% до 52%. По данным серий случаев крупных медицинских учреждений, наилучших результатов при опухолях Т1 удается достичь использованием традиционного фракционирования в дозе выше 65 Гр, при опухолях Т2 — гипофракционированием.
При распространенных, крупных опухолях чаще показана первичная хирургическая резекция, поскольку контроль опухолевого роста и сохранение функции органов при проведении нехирургического лечения часто оказываются неудовлетворительными; у таких пациентов может отмечаться рост смертности вследствие развития хронической аспирации из-за деструкции нормальных тканей опухолью или ионизирующим излучением.

В таких условиях выполнение ларингэктомии с частичной или полной фарингэктомией является обязательным, с последующим курсом адъювантной лучевой или химиолучевой терапии.
Стандартом лечения в запущенных случаях является ларингофарингэктомия с последующей послеоперационной лучевой или химиолучевой терапией. При небольших опухолях с поражением лимфоузлов, либо некрупных Т3 опухолях может использоваться химиолучевая терапия.
Альтернативной стандартной химиолучевой терапии является применение индукционной химиотерапии с последующей лучевой терапией. При такой схеме удается снизить риск развития отдаленных нарушений глотания, которые развиваются вследствие фиброзных процессов. При планировании индукционной химиотерапии проводится оценка переносимости трехкомпонентной химиотерапии TPF, поскольку использование трех препаратов повышает шанс сохранения функции гортани по сравнению со стандартной двухкомпонентной схемой.
Добавление доцетаксела к PF (цисплатину и фторурацилу) повышает вероятность сохранения гортани. Курс стандартной химиотерапии состоит из трех доз цисплатина в сочетании с семинедельным курсом лучевой терапии.
У тщательно отобранных пациентов с местно-распространенным раком, но с хорошим сохранением основных функций гортани, может использоваться комбинированная терапия с первичной химиолучевой терапией. Изолированная лучевая терапия у пациентов с Т3/Т4 или N2/N3 не позволяет добиваться хороших результатов лечения, поскольку заболевание часто персистирует. Оптимальной схемой лечения является индукционная химиотерапия с последующей лучевой или химиолучевой терапией.
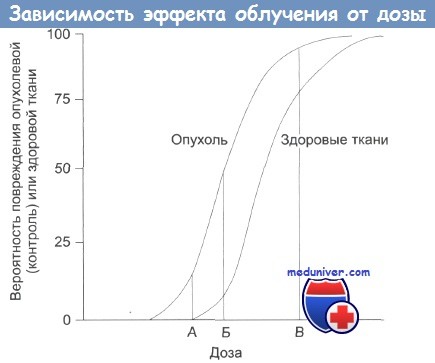
Зависимость терапевтического эффекта от дозы облучения.
А — нижняя безопасная доза;
Б — увеличение дозы: растет поражение здоровых тканей;
В — наивысшая вероятность успешного лечения, но и высокая вероятность поражения здоровых тканей, многочисленные побочные эффекты, некоторые из которых могут проявиться в отдаленном будущем
– Вернуться в оглавление раздела “отоларингология”
Оглавление темы “Отоларингология”:
- Цитология (гистология) биопсии лимфоузлов при воспалении
- Цитология (гистология) биопсии лимфоузлов при опухоли
- Цитология (гистология) биопсии наружного уха при воспалении и опухоли
- Цитология (гистология) биопсии среднего, внутреннего уха при воспалении и опухоли
- Методы лучевой терапии опухоли головы и шеи
- Варианты сочетания лучевой и химиотерапии опухоли головы и шеи
- Методы лучевой терапии при раке полости рта
- Методы лучевой терапии при раке ротоглотки
- Методы лучевой терапии при раке носоглотки
- Методы лучевой терапии при раке гортаноглотки
Источник
Методы лучевой терапии при раке ротоглотки
При раке ротоглотки на ранних стадиях обычно используется один вид лечения, которым может быть либо хирургическое удаление, либо лучевая терапия. Выбор часто основан на клиническом опыте сотрудников конкретного лечебного учреждения или на предполагаемом функциональном исходе.
Химиотерапия при раке ротоглотки ранних стадий используется редко. Исход в большинстве случаев благоприятный, излечения удается достичь у 90% больных. С помощью традиционного фракционного облучения можно добиться превосходного контроля роста опухолей стадии Т1, но его может оказаться недостаточно для лечения рака корня языка и задней стенки глотки стадии Т2.
Исследование эффективности традиционного фракционированного облучения при раке небных миндалин оценивалось в нескольких крупных одноцентровых сериях случаев, согласно которым местного контроля удается достичь после проведения традиционного фракционированного облучения (разовая доза 1,8-2 Гр в течение 6,5-7 недель до 65-70 Гр) примерно в 80-90% опухолей Т1 и Т2, 63-74% в стадии ТЗ.
а) Ипсилатеральная наружная дистанционная терапия при раке небных миндалин ранних стадий. Как правило, при опухолях стадий Т1 и Т2, расположенных на латеральной стенке глотки, у пациентов со статусом лимфоузлов N0 или N1, могут использоваться ипсилатеральные поля облучения. Если новообразование пересекает среднюю линию, поражает корень языка или мягкое небо, сопровождается поражением лимфоузлов N2 и более, следует проводить полное двустороннее облучение.
При использовании такого подхода в некоторых случаях удается избежать повреждения противоположной слюнной железы, снизив, таким образом, риск развития ксеростомии. Согласно данным Eisbruch и соавт., пациенты, у которых облучение проводилось лишь с одной стороны, имели более высокое качество жизни по сравнению с теми, кому проводилась двухсторонняя ЛТМИ, не затрагивающая противоположную слюнную железу.
На ранних стадиях многие опухоли мягкого неба и глотки расположены около средней линии, что увеличивает риск двустороннего поражения лимфоузлов шеи и заглоточных лимфоузлов. Поэтому в данных случаях предпочтительно использовать наружную дистанционную лучевую терапию, при помощи которой удается добиться контроля опухолей Т1 и Т2 стадий (аналогично раку небных миндалин).
Лучевая терапия не сопровождается появлением небно-глоточной недостаточности с забросом пищи и жидкости в носоглотку и полость носа, больным не приходится использовать специальные обтураторы. Согласно результатам крупных одноцентровых серий случаев, при помощи лучевой терапии можно добиться высокой степени контроля местно-регионарного роста опухоли.

б) Лечение местно-распространенного операбельного рака стадий III и IV. Изолированная лучевая терапия может быть эффективной у пациентов с новообразованиями промежуточных стадий (TI/T2N1 или Т3N0). Но при операбельных распространенных опухолях Т3-Т4, либо при массивном поражении лимфоузлов N2 и N3 изолированная лучевая терапия с меньшей вероятностью приводит к достижению благоприятного результата, чем комбинированное лечение.
Большинство пациентов с раком ротоглотки обращаются за медицинской помощью в стадии III—IV, поэтому им практически всегда требуется комбинация хирургического, лучевого и химиотерапевтического лечения. Часто выбор метода лечения зависит от опыта и предпочтений медицинской бригады. Возможны следующие варианты лечения:
(1) хирургическое удаление с последующей лучевой или химиолучевой терапией;
(2) химиолучевая терапия, которая, по мнению многих специалистов, является стандартом лечения пациентов с местно-распространенным раком ротоглотки. Наиболее изученным препаратом является циспластин, который вводится болюсно в дозе 100 мг/м2 каждые три недели во время лучевой терапии. Пациенты, которые не могут переносить такую дозировку и схему введения цисплатина, обычно каждую неделю получают паклитаксел/карбоплатин, цисплатин или цетуксимаб;
(3) последовательная индукционная терапия с последующей лучевой или химиолучевой терапией. В качестве индукционной терапии наиболее часто используется TPF (доцетаксел+цисплатин+фторурацил) каждые три недели в течение трех курсов. Затем проводится либо курс лучевой терапии, либо лучевой терапии в сочетании с еженедельным приемом карбоплатина.
У пациентов с опухолями Т4 или N3 используется либо химиолучевая терапия, либо последовательная индукционная химиотерапия с последующей химиолучевой терапией. Последовательная химиотерапия используется только в случае хорошего общего состояния больного, поскольку у данной группы пациентов прогноз значительно хуже, чем у пациентов с операбельными опухолями. Пятилетний уровень излечения составляет 25-40%.
в) Рак ротоглотки, ассоциированный с вирусом папилломы человека. В последнее время стала ясна роль вируса папилломы человека, особенно ВПЧ-16, в качестве одного из главных факторов риска рака ротоглотки в странах Запада. Считается, что на настоящий момент около 50-60% случаев рака ротоглотки связано с ВПЧ. Основные признаки данной формы заболевания:
• Пациенты в среднем на 10 лет моложе тех, у кого рак ротоглотки развился вследствие курения или употребления алкоголя. Многим пациентам с раком ротоглотки, вызванным ВПЧ, от 40 до 50 лет.
• В большинстве случаев пациенты не курят и не злоупотребляют алкоголем.
• При осмотре определяется небольшой первичный очаг и выраженная лимфаденопатия.
• При микроскопии определяется «базалоидный» вид опухоли.
• Прогноз благоприятный. Даже при местно-распространенных формах вероятность излечения может достигать 85-90%. Из-за этого в настоящий момент многие клинические исследования изучают именно данную группу пациентов. До тех пор, пока данные исследования не будут завершены, лечение не должно зависеть от ВПЧ-статуса.
ВПЧ-статус устанавливается либо посредством флуоресцентной гибридизации in situ (FISH), либо посредством полимеразной цепной реакции (ПЦР). В качестве альтернативного метода можно использовать иммуногистохимический анализ на р16 для косвенного подтверждения ВПЧ и ВИЧ-статуса. Материалом для всех данных исследований является операционный препарат. Поскольку ВПЧ-статус имеет важное прогностическое значение, его рекомендуется оценивать у всех больных с раком ротоглотки.
г) Брахитерапия при раке ротоглотки. Не одно десятилетие брахитерапия оставалась основным методом лечения рака ротоглотки с сообщениями о превосходных результатах. Брахитерапия, т.е. внедрение радиоактивного источника непосредственно в опухоль, позволяет обеспечить повышение дозы облучения, получаемой тканью опухоли, но при этом добиться уменьшения облучения нормальных тканей пропорционально обратным квадратам расстояния от источника.
Также уменьшить повреждения нормальных тканей удается за счет того, что использование брахитерапии позволяет снизить общую дозу лучевой терапии, что особенно важно у пациентов, также получающих химиотерапию.
Несколько лечебных учреждений опубликовали результаты успешного лечения опухолей корня языка при помощи данного подхода. Также было выявлено, что использование брахитерапии чаще сопровождается сохранением нормального глотания (по сравнению с изолированной наружной дистанционной лучевой терапией).
– Также рекомендуем “Методы лучевой терапии при раке носоглотки”
Оглавление темы “Отоларингология”:
- Цитология (гистология) биопсии лимфоузлов при воспалении
- Цитология (гистология) биопсии лимфоузлов при опухоли
- Цитология (гистология) биопсии наружного уха при воспалении и опухоли
- Цитология (гистология) биопсии среднего, внутреннего уха при воспалении и опухоли
- Методы лучевой терапии опухоли головы и шеи
- Варианты сочетания лучевой и химиотерапии опухоли головы и шеи
- Методы лучевой терапии при раке полости рта
- Методы лучевой терапии при раке ротоглотки
- Методы лучевой терапии при раке носоглотки
- Методы лучевой терапии при раке гортаноглотки
Источник